Bersaglio classico di danno cellulare è l’ATP. L’ATP è la benzina della cellula e serve per numerosi processi: sintesi proteica, trasporto di membrana, metabolismo dei lipidi e molto altro. La deplezione di ATP è quindi un meccanismo primario di danno cellulare. L’ATP può essere prodotto tramite due processi:
- Fosforilazione ossidativa: produzione di ATP a livello mitocondriale, si associa la riduzione di ossigeno ad acqua nella catena respiratoria e alla produzione di ATP a partire da ADP.
- Glicolisi: tramite fosforilazione a livello del substrato si può ottenere ATP da glucosio e glicogeno (previa sua degradazione a glucosio).
La deplezione di ATP si verifica a seguito di ischemia o di intossicazione da tetracloruro di carbonio (CCl4), barbiturici, paracetamolo (questi ultimi sono classificati come danno tossico, e quindi chimico).
La glicolisi avviene sempre, sia in condizioni aerobiche che anaerobiche nel citoplasma. Il glucosio viene demolito a due molecole di piruvato, due di ATP e due di NADH in seguito ad una serie di reazioni, perché se venisse trasformata in una sola reazione la cellula si brucerebbe (perché l’energia associata a questo processo sarebbe troppo elevata); invece c’è l’accoppiamento di reazioni graduali che permettono di avere substrati per altre reazioni e anche energia. In condizioni aerobiche il piruvato viene decarbossilato in Acetil-CoA, entra nel ciclo di Krebs, ed avviene la fosforilazione ossidativa, mentre in condizioni anaerobiche il piruvato viene convertito in lattato (fermentazione omolattica), ciò che avviene inizialmente in un cardiomiocita infartuato.
Nel ciclo di Krebs è possibile completare l’ossidazione del piruvato ad anidride carbonica e tramite la fosforilazione ossidativa liberare molto più ATP di quanto non se ne possa ottenere dalla sola glicolisi in condizioni anaerobiche. Nelle varie fasi del ciclo di Krebs, infatti, vengono prodotti NADH e FADH2, trasportatori di elettroni che partecipano alla catena respiratoria cedendo elettroni e ottenendo infine la riduzione dell’ossigeno ad acqua.
Fonte: Le basi patologiche delle malattie.
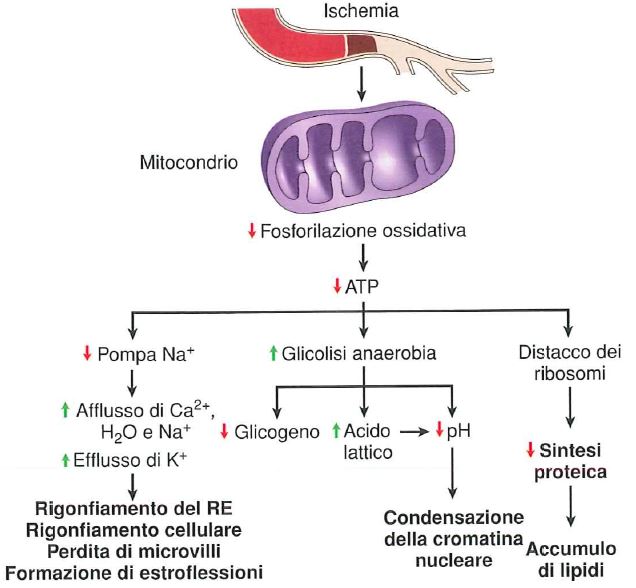
Quando la deplezione di ATP è al di sotto del 10% si ha un evento ischemico, si verifica una riduzione della fosforilazione ossidativa (perché c’è meno ossigeno), la quota di ATP che può venire prodotta dalla cellula stessa si riduce, e nel contempo essa non viene rifornita di nutrienti. La riduzione della quota di ATP genera una inibizione di tutti i meccanismi cellulari che lo utilizzano con conseguente danno cellulare.
La glicolisi da sola può produrre ATP in quantità sufficienti solo per un breve intervallo di tempo, che tra l’altro dipende dal citotipo considerato e dalle quantità di glicogeno immagazzinato in cellula.
Il danno dovuto a deplezione di ATP è particolarmente evidente a carico della pompa sodio-potassio, la quale smette di funzionare, con conseguente ingresso di acqua nella cellula. Si ha anche ingresso di calcio (le pompe per il calcio che lo sequestrano nel reticolo endoplasmatico liscio e quelle che lo pompano all’esterno della cellula smettono di funzionare) ed efflusso di potassio.
Di conseguenza la cellula si gonfia, lo stesso fa il reticolo endoplasmatico, i ribosomi si staccano dal reticolo endoplasmatico, si formano i “blebs” e scompaiono i microvilli, mentre aumenta la glicolisi anaerobia (“per salvare il salvabile”) e viene attivata la glicogeno fosforilasi con conseguente demolizione di glicogeno e liberazione di glucosio usato per la glicolisi anaerobia. Ciò tuttavia porta ad accumulo di acido lattico e riduzione del pH cellulare. L’abbassamento del pH porta ad un addensamento della cromatina nel nucleo. Inoltre, il distacco di ribosomi dal reticolo endoplasmatico rugoso provoca riduzione della sintesi proteica e viene inibita la sintesi degli enzimi necessari per produrre i fosfolipidi di membrana, con conseguente danno anche alla membrana cellulare.
Vi è pertanto una interconnessione tra vari elementi che portano ad un danno cellulare serio.


