Tutto ciò che ci circonda è materia. La scienza che studia le proprietà e trasformazioni di tutte le forme di materia è chiamata chimica.
La materia è formata tutta dalla stessa unità di base, gli atomi (particelle infinitamente piccole).
Alla fine del XIX secolo, gli scienziati credevano che la materia fosse solo costituita da atomi, e pensavano che l’atomo fosse la più piccola particella costitutiva. Nel 1911, Ernest Rutherford descrisse la struttura interna dell’atomo. Con i suoi esperimenti si scoprì che all’interno dell’atomo c’era un nucleo centrale, attorno al quale ruotavano gli elettroni, particelle con carica elettrica negativa. Il nucleo, a sua volta, è formato da protoni, particelle con carica elettrica positiva, e da neutroni, particelle elettricamente neutre.
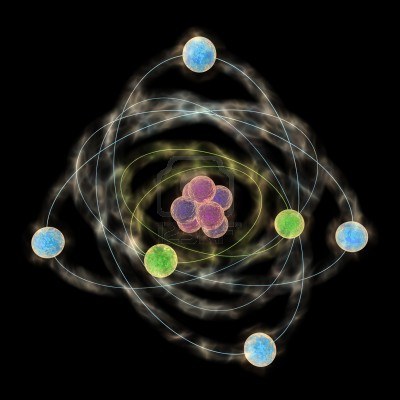
Questo modello atomico è noto come modello planetario perché ricorda il Sistema Solare.
Il modello planetario dell’atomo fu in seguito sostituito da un nuovo modello, chiamato modello quantomeccanico. Secondo questo modello, gli elettroni non ruotano attorno al nucleo su orbite definite; il loro comportamento è descritto da orbitali. Un orbitale è una regione di spazio intorno al nucleo, all’ interno della quale esiste la massima probabilità di trovare un elettrone.
Gli orbitali sono raggruppati in strati detti livelli energetici, che hanno un contenuto di energia maggiore via via che ci si allontana dal nucleo. In tutti gli atomi gli elettroni riempiono gli orbitali partendo da quello più interno, dotato di minore energia, a quello più esterno che è quello che determina le proprietà chimiche di un elemento, cioè il suo comportamento durante le reazioni.

