La scintigrafia epatobiliare (nota anche come colescintigrafia) è una procedura di imaging diagnostico in medicina nucleare che valuta la funzione epatocellulare e la corretta pervietà/funzionamento della via biliare escretoria, tracciando la produzione e il flusso della bile dalla sua produzione nel fegato fino al suo passaggio attraverso il sistema biliare nell’intestino tenue.
Dall’inizio degli anni ’80, la scintigrafia epatobiliare è un prezioso test diagnostico clinico ampiamente disponibile nei centri di medicina nucleare. Se eseguita in modo ottimale, la scintigrafia epatobiliare è un metodo sensibile per rilevare vari disturbi del fegato e del sistema biliare. Ulteriori test farmacologici possono migliorare l’utilità diagnostica della scintigrafia epatobiliare e fornire la valutazione quantitativa necessaria per alcune applicazioni specifiche.
Anatomia e fisiologia
Il fegato è il secondo organo più grande del corpo umano, con un peso di 1.200-1.500 g, circa il 4-5% del peso corporeo. Si trova nel quadrante addominale superiore destro, o nelle regioni ipocondriaca destra ed epigastrica, dietro le coste inferiori.
Il legamento falciforme divide anatomicamente il fegato in due lobi disuguali: destro e sinistro. Due ulteriori lobi più piccoli, il lobo quadrato e il lobo caudato, sono più visibili in sezione trasversale. Fisiologicamente, però, la divisione è equa, seguendo la fossa della cistifellea e la vena cava inferiore. Non vi è evidenza di differenze funzionali tra i quattro lobi anatomici.
La cistifellea, o colecisti, è un organo sacculare a forma di pera situato posteriormente alla parte più anteriore del fegato e ha la funzione di immagazzinare la bile. Ha una capacità media di 30-50 mL. Le pieghe mucose, chiamate valvole spirali di Heister, mantengono la pervietà del dotto cistico per consentire il passaggio della bile.
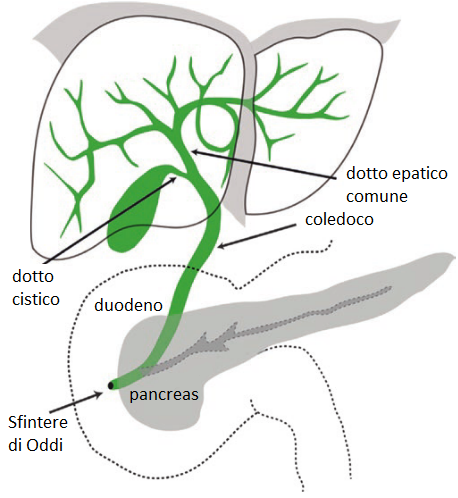
La bile viene sintetizzata e secreta dagli epatociti nei canalicoli biliari, per poi fluire in dotti progressivamente più grandi che formano i dotti epatici destro e sinistro. Questi dotti si uniscono infine nel dotto epatico comune. Il dotto epatico comune si unisce poi con il dotto cistico proveniente dalla colecisti per formare il dotto biliare comune, attraverso il quale la bile raggiunge il duodeno tramite la papilla duodenale maggiore (di Vater). Tuttavia, non tutta la bile fluisce direttamente nel duodeno. Circa il 50% della bile prodotta dal fegato viene prima immagazzinata nella cistifellea.
Quando viene ingerito del cibo, in particolare quando i lipidi raggiungono il duodeno, la cistifellea si contrae e rilascia la bile immagazzinata per aiutare la digestione e l’assorbimento dei grassi. Le principali funzioni del sistema biliare sono:
- drenare i prodotti di scarto dal fegato nell’intestino;
- aiutare la digestione con il rilascio controllato della bile.
La bile è un fluido giallo-verde (composto da prodotti di scarto, colesterolo e sali biliari). I sali biliari sono i componenti che effettivamente aiutano a scomporre e ad assorbire i grassi.
Radiofarmaci e tecnica
Il primo agente colescintigrafico clinicamente utile fu il 131I-rosa bengala; tuttavia, la qualità dell’immagine era relativamente scarsa e attualmente, questo agente ha solo rilevanza storica, anche se si passa da 131I a 123I.
I radiofarmaci epatobiliari marcati con tecnezio (99mTc) furono scoperti per caso. Durante le indagini per un radiofarmaco di imaging cardiaco, si scoprì che la lidocaina marcata con 99mTc non era un buon agente di imaging cardiaco, ma veniva eliminata rapidamente attraverso il sistema epatobiliare. Con alcune modifiche chimiche, furono sviluppati agenti di imaging epatobiliare marcati con 99mTc e iniziarono ad essere ampiamente utilizzati all’inizio degli anni ’80.
Il primo radiofarmaco epatobiliare marcato con 99mTc, l’acido iminodiacetico (HIDA), fu approvato per l’uso clinico dalla FDA nel 1982. Il 99mTc-dimetil (2,6-diisopropilacetanilido iminodiacetico) costituì un importante avanzamento, ma la qualità delle immagini e l’utilità diagnostica erano subottimali nei pazienti con livelli di bilirubina sierica superiori a 5,0 mg/dL. Questo agente non è più disponibile in commercio.
Nel 1986, la FDA approvò il 99mTc-disofenin (acido diisopropil iminodiacetico), che fornisce immagini di qualità diagnostica anche con livelli di bilirubina fino a 25–30 mg/dL.
Nel 1993, fu approvato il 99mTc-mebrofenin (bromo-2,4,6-trimetilacetanilido iminodiacetico, TBIDA), basato su una maggiore estrazione epatica (98% rispetto all’89%) e una clearance biliare più rapida rispetto al 99mTc-disofenin (emivita di 17 minuti rispetto a 19 minuti).
Il 99mTc-disofenin o il 99mTc-mebrofenin vengono somministrati per via endovenosa in dosi di 111–185 MBq (3–5 mCi) per adulti; una dose maggiore può essere necessaria nei pazienti con iperbilirubinemia. Il 99mTc-mebrofenin può essere scelto invece del 99mTc-disofenin nei pazienti con disfunzione epatica da moderata a grave, a causa della sua maggiore estrazione epatocellulare.
La dose somministrata per neonati e bambini è di 1,8 MBq/kg (0,05 mCi/kg), con una dose minima di 18,5 MBq (0,5 mCi). Il 99mTc-mebrofenin è sempre preferito nei neonati con iperbilirubinemia, con una dose minima di 37 MBq (1,0 mCi), poiché spesso sono necessarie immagini tardive fino a 24 ore.
Dopo l’iniezione endovenosa, i radiofarmaci HIDA marcati con 99mTc vengono trasportati nel sangue legati all’albumina sierica. Si dissociano dall’albumina nello spazio perisinusoidale epatico e vengono estratti dagli epatociti mediante endocitosi mediata da recettore, similmente ai sali biliari, agli acidi grassi liberi e alla bilirubina. Segue lo stesso percorso metabolico della bilirubina, eccetto che vengono secreti nei canalicoli biliari senza subire coniugazione. Circa due terzi del tracciante entra nella cistifellea tramite il dotto cistico, mentre il resto esce nella seconda parte del duodeno tramite il dotto biliare comune e lo sfintere di Oddi.
La distribuzione del tracciante nel sistema biliare dipende dalla pervietà dei dotti biliari, dalle pressioni intraluminali e dal tono dello sfintere di Oddi, pertanto, una distribuzione anomala è indice di alterazione di uno di questi sistemi.

Preparazione del paziente
Tutte le informazioni cliniche, di laboratorio e di imaging disponibili (ad esempio, ecografia, risonanza magnetica, se adeguate) dovrebbero essere riviste prima della scansione. Le informazioni aggiuntive specificamente correlate alla scintigrafia epatobiliare dovrebbero includere:
- storia di interventi chirurgici precedenti, in particolare biliari e gastrointestinali;
- orario dell’ultimo pasto;
- farmaci attualmente assunti, con particolare attenzione agli oppioidi;
- livelli recenti di bilirubina e enzimi epatici;
- ecografia della cistifellea o addominale.
Per consentire una rapida visualizzazione della cistifellea, il paziente adulto deve aver digiunato per un minimo di 2 ore e preferibilmente 6 ore prima della somministrazione del radiofarmaco. I bambini dovrebbero essere istruiti a digiunare per 2-4 ore, mentre i neonati devono digiunare solo 2 ore prima dell’iniezione del radiotracciante. In quest’ultimo gruppo, sono permessi liquidi chiari (senza latte), se necessari dal punto di vista medico.
Tuttavia, il digiuno per più di 24 ore (inclusi quelli in nutrizione parenterale totale) può causare il mancato riempimento della colecisti con radioattività entro il tempo normalmente previsto. In questo caso il paziente può essere pretrattato con sincalide che determina una contrazione della colecisti.
La mancata osservanza delle precauzioni sopra citate può determinare una falsa non visualizzazione della cistifellea. L’interferenza degli oppioidi può essere minimizzata ritardando lo studio per un tempo corrispondente a 4 emivite del farmaco. In alcuni casi l’effetto può essere invertito con naloxone cloridrato.
Acquisizione delle immagini
Si raccomanda l’uso di una gamma-camera con ampio campo visivo equipaggiata con un collimatore a bassa energia adatto a tutti gli usi o ad alta risoluzione. Quando possibile, si dovrebbe eseguire un’acquisizione continua (dinamica) tramite computer (solitamente in vista anteriore o obliqua anteriore sinistra) (1 fotogramma/min). Una matrice di 128 × 128 (con fattore di zoom 1) è ottimale per una gamma-camera a campo visivo ampio standard. Nei pazienti pediatrici si dovrebbe utilizzare uno zoom elettronico appropriato.
Le immagini iniziali sono solitamente acquisite in modalità dinamica, a partire dall’iniezione e continuando per 60 minuti.
Quando la visualizzazione della cistifellea è l’obiettivo finale dello studio, l’acquisizione può essere interrotta prima, non appena l’attività è visibile nella cistifellea. Ulteriori viste (ad esempio, laterale destra, obliqua anteriore sinistra o destra) possono essere ottenute se necessario, per chiarire l’anatomia.
La visualizzazione dell’attività del tracciante nell’intestino tenue può risolvere il dubbio di ostruzione del dotto biliare comune (altamente improbabile in presenza di visualizzazione della cistifellea).
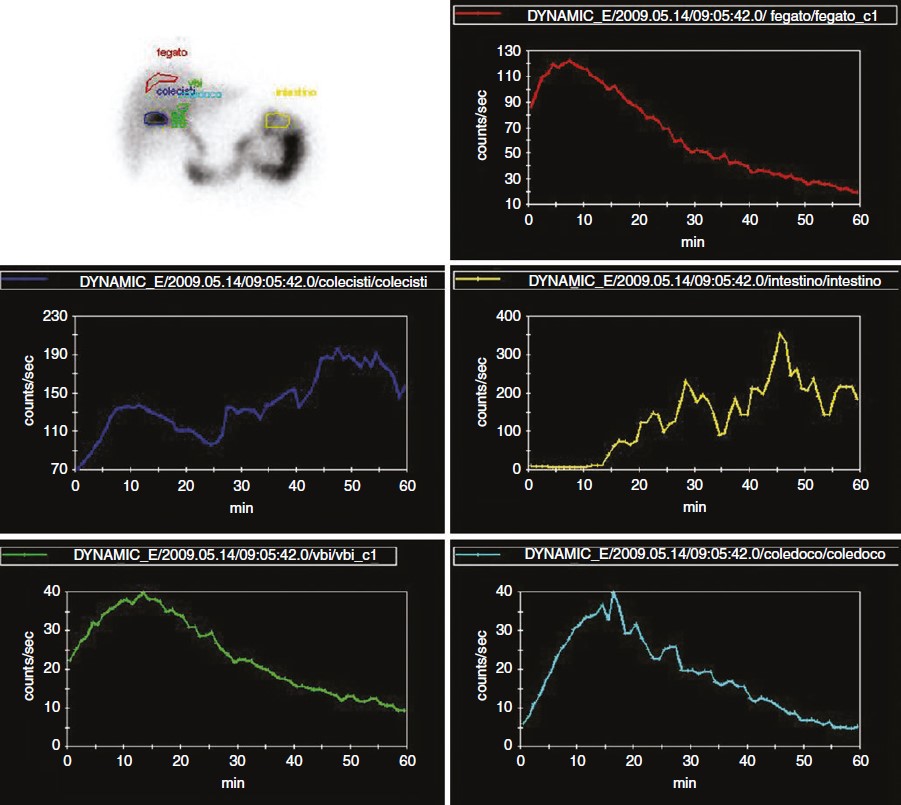
Le curve tipiche di attività/tempo corrispondenti alle regioni di interesse (ROIs) definite sulle principali strutture visualizzate durante la registrazione dinamica della scintigrafia epatobiliare in un soggetto sano, senza disfunzione epatocellulare o biliare, sono rappresentate nella figura accanto. In questi soggetti, il radiotracciante dovrebbe concentrarsi nel fegato ed essere eliminato dal pool sanguigno cardiaco entro circa 5 minuti. La persistenza dell’attività nel pool sanguigno oltre i 20 minuti indica una ridotta funzione epatocellulare, che può essere dovuta a cause di insufficienza epatica o malattie intercorrenti.
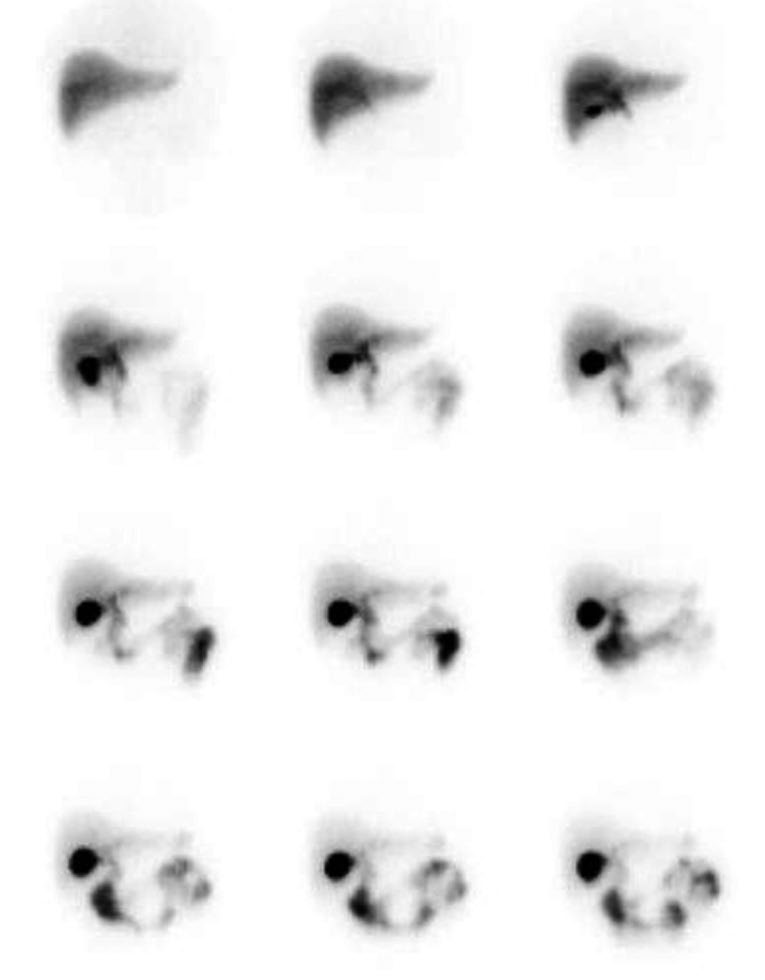
La radioattività è normalmente visibile nei dotti biliari tra i 10 e i 30 minuti e nell’intestino entro 60 minuti dall’iniezione del radiofarmaco 99mTc-HIDA (vedi figura accanto). Si osserva una rapida visualizzazione del parenchima epatico nella fase iniziale di assorbimento e concentrazione del radiofarmaco 99mTc-HIDA. La colecisti è visualizzata intorno ai 15 minuti e la radioattività escreta inizia ad accumularsi nell’intestino già intorno ai 20 minuti. Non si osserva stasi di radioattività nei principali dotti biliari intra- ed extraepatici. I fotogrammi successivi mostrano una quasi completa eliminazione della radioattività dal parenchima epatico, con la cistifellea completamente distesa con bile radioattiva (questo sarebbe un momento adeguato per stimolare lo svuotamento della cistifellea indotto sia da un pasto grasso sia dalla somministrazione dell’analogo della colecistochinina, la sincalide).
I pazienti pretrattati con sincalide possono avere un ritardo più lungo prima che l’attività del radiotracciante sia visibile nell’intestino. Questo è probabilmente dovuto all’accumulo preferenziale del radiotracciante in una cistifellea vuota. Tuttavia, se la clearance parenchimale e i tempi di transito del radiotracciante nell’intestino sono gravemente prolungati, si dovrebbe considerare un’ostruzione biliare. Questo può verificarsi quando c’è un calcolo nel dotto biliare comune in caso di colecistite acuta calcolosa, causando ostruzione.
Indicazioni cliniche
La scintigrafia epatobiliare è utilizzata in modo appropriato in molti scenari clinici; le indicazioni cliniche più comuni includono:
- sindromi di dolore biliare funzionale negli adulti e nei pazienti pediatrici;
- colecistite acuta;
- varianti di dolore in ipocondrio destro;
- pervietà del sistema biliare;
- perdita di bile;
- iperbilirubinemia neonatale (atresia biliare rispetto alla sindrome di epatite neonatale);
- valutazione del bypass bilio-enterico (ad esempio, procedura di Kasai);
- valutazione del trapianto di fegato;
- sindrome del loop afferente;
- valutazione delle cisti coledocali;
- calcolo della frazione di eiezione della cistifellea (GBEF);
- valutazione funzionale del fegato prima della resezione epatica parziale;
- dimostrazione di lobulazione anomala del fegato;
- valutazione del reflusso enterogastrico (duodeno-gastrico);
- reflusso biliare esofageo dopo gastrectomia;
- disfunzione dello sfintere di Oddi.
Fonte: Fondamenti di medicina nucleare. Tecniche e applicazioni.