Lo stravaso rappresenta un effetto indesiderato correlato all’iniezione parenterale di un medicinale. Si definisce come l’accidentale infiltrazione di un liquido o di un farmaco dal sito di iniezione al tessuto sottocutaneo circostante o verso tessuti più lontani dal punto d’iniezione. Più in generale, il termine stravaso si riferisce sia al passaggio del farmaco iniettato dalla vena ai tessuti circostanti, sia alle conseguenze in termini di lesioni causate da questo passaggio tissutale del farmaco.
Le tecniche di imaging di Medicina Nucleare hanno aperto la strada alla conoscenza approfondita di numerose patologie mediante le applicazioni mediche dei radionuclidi. Questi si distinguono, in base al tipo di radiazione emessa, in radionuclidi diagnostici e radionuclidi terapeutici.
- Radionuclidi per diagnostica: comprendono tutti quei radionuclidi per i quali, durante il processo di decadimento, si osserva l’emissione di fotoni, principalmente sotto forma di raggi gamma. Questi hanno una bassa probabilità di interazione con la materia (e di conseguenza con le strutture cellulari) e una minima dose assorbita dal paziente;
- radionuclidi per terapia: comprendono gli emettitori di particelle β- e α che, a causa dell’elevata capacità di interazione con la materia, inducono un danno irreversibile. Questo può essere sfruttato a scopo terapeutico in seguito all’accumulo selettivo all’interno di un particolare tessuto.
La maggior parte degli esami diagnostici di medicina nucleare e delle infusioni terapeutiche viene eseguita mediante la somministrazione di radiofarmaci per via endovenosa. Lo stravaso è un fenomeno che si verifica relativamente di frequente, con una media del 10,4%. Il tasso medio di stravaso osservato in una revisione pubblicata recentemente corrisponde a circa l’8%. Utilizzando la definizione della European Medical Association per gli effetti avversi, il verificarsi di un evento compreso tra l’1% e il 10% sarebbe considerato “comune”. Supponendo che le stime recenti per le procedure diagnostiche di imaging nucleare siano corrette (13,5 milioni), ciò indica che circa un milione di pazienti all’anno potrebbero manifestare un evento di stravaso.
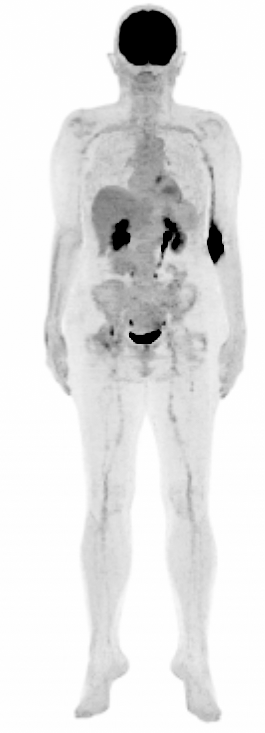
Storicamente, questo evento è stato considerato di scarsa importanza nell’imaging molecolare, tanto che lo stravaso e l’infiltrazione di radiofarmaci non sono classificati come eventi medici e sono esentati dall’obbligo della segnalazione, a meno che non soddisfino specifici criteri (Nuclear Regulatory Commission, NRC).
L’emergere e l’adozione diffusa di nuove terapie con radionuclidi ha portato però a una maggiore consapevolezza riguardo all’impatto della somministrazione dei radiofarmaci, sia diagnostici che terapeutici. Data la loro natura radioattiva, lo stravaso di radiofarmaci può comportare una dose significativa ai tessuti sottostanti e alla pelle. Gli effetti dello stravaso possono essere correlati a conseguenze anche gravi, soprattutto per i radiofarmaci a scopo terapeutico, accompagnati da un ritardo di insorgenza dell’effetto indesiderato da pochi giorni a diverse settimane, oltre che a un rischio attribuibile alla radioattività. Quest’ultimo dipende dal tipo di radiazione emessa, dall’energia e dall’emivita del radionuclide ed è responsabile dell’insorgenza di danni tissutali, difficili da prevedere, in funzione della dose, del volume stravasato e dell’intensità della radiazione emessa.
Poiché gli effetti delle radiazioni sui pazienti possono richiedere anni per manifestarsi e sono raramente studiati, il fenomeno dello stravaso necessita di attenzione e deve essere valutato in modo più completo.
Classificazione dello stravaso
A seconda del tipo di reazione che inducono in caso di stravaso e dell’intensità del danno tissutale generato, i farmaci possono essere raggruppati in tre grandi categorie:
- agenti irritanti: possono causare dolore e/o infiammazione nel punto di iniezione e oltre. Alcuni di questi agenti sono suscettibili di indurre ulcerazione se una quantità significativa del farmaco si diffonde nel tessuto;
- agenti non vescicanti: non causano necrosi o ulcerazione;
- agenti vescicanti: possono causare ulcerazioni o addirittura necrosi tissutali.
In ambito radiofarmaceutico, i radiofarmaci a scopo terapeutico sono classificabili come agenti vescicanti, mentre quelli a scopo diagnostico sono considerati irritanti, a seconda del livello di radiotossicità dei loro radionuclidi.
| Radionuclide | Tipo di radiazione emessa (maggioranza) | Livello di radiotossicità | Utilizzo |
|---|---|---|---|
| 99mTc | γ | Debole | Diagnostico |
| 123I | γ | Debole | Diagnostico |
| 51Cr | γ | Debole | Diagnostico |
| 67Ga | γ | Moderato | Diagnostico |
| 111In | γ | Moderato | Diagnostico |
| 18F | β+ | Moderato | Diagnostico |
| 125I | γ | Moderato | Diagnostico |
| 201Tl | γ | Moderato | Diagnostico |
| 68Ga | β+ | Forte | Diagnostico |
| 131I | β-/γ | Moderato | Diagnostico/Terapeutico |
| 169Er | β-/γ | Debole | Terapeutico |
| 186Re | β-/γ | Moderato | Terapeutico |
| 89Sr | β- | Moderato | Terapeutico |
| 153Sm | β-/γ | Moderato | Terapeutico |
| 90Y | β- | Forte | Terapeutico |
| 223Ra | α | Forte | Terapeutico |
Fattori di rischio specifici per lo stravaso di radiofarmaci
L’impatto e le conseguenze dello stravaso di radiofarmaci dipendono principalmente dalla natura del radionuclide, che può essere diagnostico o terapeutico.
Nella pratica diagnostica medico-nucleare, lo stravaso è spesso sottostimato e poco documentato. Questo avviene perché gli effetti sul paziente sono generalmente limitati: i volumi somministrati sono ridotti a pochi millilitri e l’energia e il tempo di decadimento dei radionuclidi diagnostici non comportano una significativa esposizione alle radiazioni. La gestione dello stravaso è spesso lasciata al “buon senso” clinico, con azioni estemporanee e non proceduralizzate.
In oncologia e radiologia, il problema dello stravaso causato dall’infusione di chemioterapici o mezzi di contrasto è ampiamente affrontato. Tuttavia, lo stesso non avviene per i radiofarmaci diagnostici, nonostante il loro impatto sulla corretta esecuzione di esami come PET o scintigrafie e, di conseguenza, sull’inquadramento clinico del paziente (diagnosi, stadiazione, valutazione della risposta metabolica al trattamento antineoplastico).
La mancata valutazione di uno stravaso di radiofarmaci diagnostici può portare a una sottostima dei valori di assorbimento (SUV) dal 10% fino al 21-50%, e nei casi estremi, a una errata o mancata identificazione di lesioni, con conseguente diagnosi imprecisa ed errata valutazione clinica del paziente.
A causa dei bassi volumi somministrati, può essere difficile rilevare uno stravaso di un radiofarmaco diagnostico. Tuttavia, una volta identificato, è fondamentale una presa in carico immediata del paziente e una valutazione degli effetti sull’imaging.
Lo stravaso di un radiofarmaco e la gravità del danno associato possono essere influenzati da vari fattori:
- Errori nella tecnica di somministrazione;
- Errori nei dispositivi di somministrazione;
- Fattori legati al paziente;
- Caratteristiche chimico-fisiche del radiofarmaco.
L’eliminazione dell’errore umano è impossibile, ma il rischio può essere minimizzato attraverso un buon training degli operatori, sia con corsi di preparazione che con formazione continua. È essenziale che l’operatore conosca le caratteristiche del radiofarmaco, il tipo di radiotossicità locale, i tempi e le modalità di somministrazione. Deve inoltre saper gestire i diversi accessi venosi e utilizzare correttamente i presidi di infusione.
I pazienti che hanno ricevuto precedenti chemioterapie o radioterapie sono a maggior rischio di stravaso a causa dell’indurimento della zona da pungere e della sclerosi venosa. Altri fattori predisponenti includono aree di somministrazione trattate chirurgicamente, alta percentuale di tessuto fibrotico, e maggiore fragilità cutanea e venosa nei bambini e negli anziani.
La capacità di collaborazione del paziente è cruciale, così come la sua informazione e istruzione sul riconoscimento immediato dei segni e sintomi dello stravaso.
Il volume e il tempo di somministrazione sono variabili importanti: un aumento di questi fattori è direttamente proporzionale al rischio di dislocamento dell’ago. Si consiglia di posizionare i dispositivi di somministrazione in punti facilmente osservabili e di evitare vene fragili o in zone con circolo compromesso.
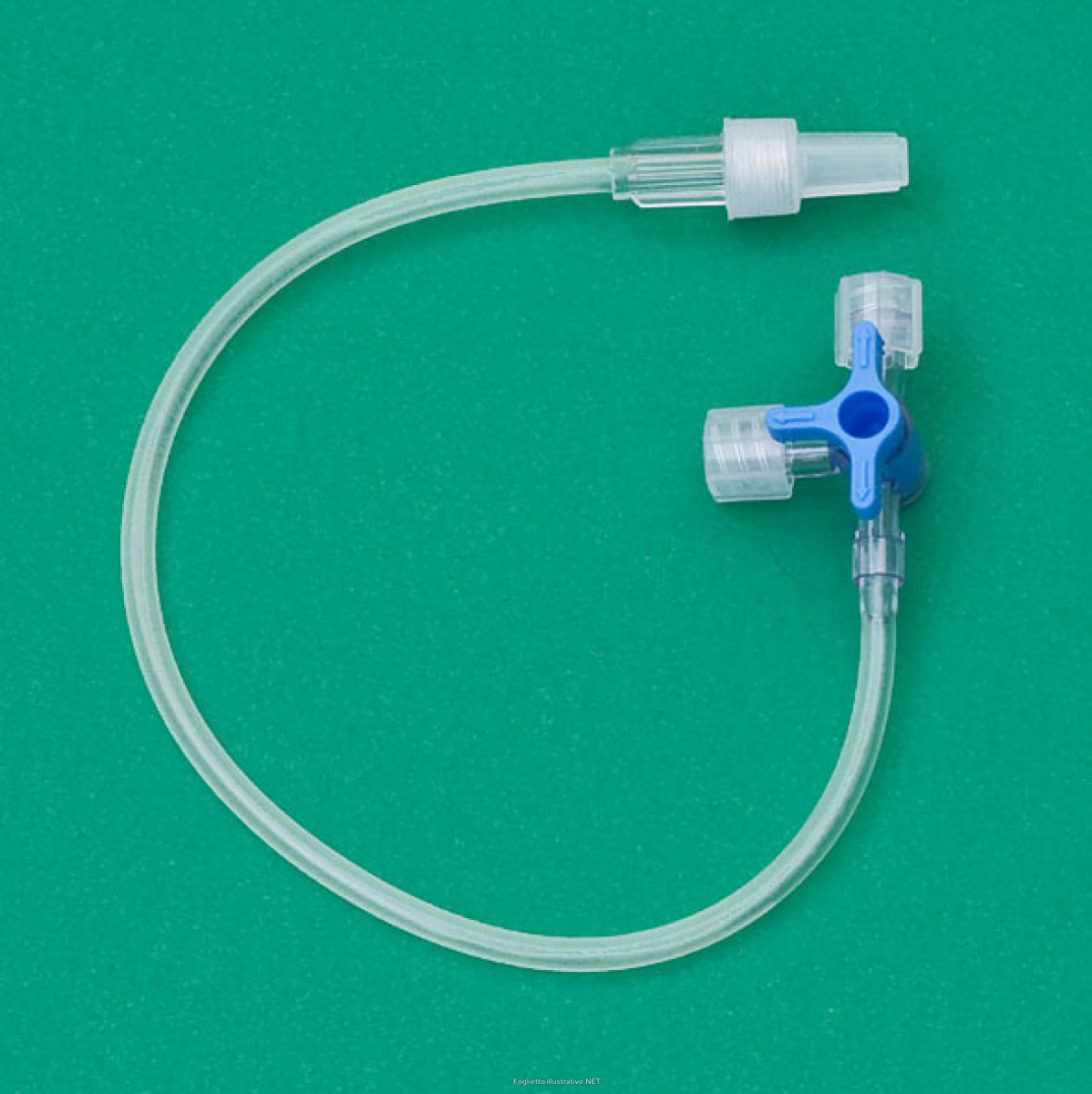
Raccomandazioni:
- Evitare l’uso di zone anatomiche come giunture e pieghe;
- Non coprire il punto d’inserzione con cerotto, preferendo medicazioni in poliuretano trasparente;
- Utilizzare raccordi luer-lock ad Y e rubinetti a tre vie per somministrare una soluzione di lavaggio della vena;
- Schermare adeguatamente la siringa per consentire una buona visibilità del ritorno venoso.
A causa del rischio di gravi conseguenze in caso di stravaso, la somministrazione di radiofarmaci terapeutici richiede l’inserimento sistematico di un catetere venoso, che deve essere testato controllando il ritorno venoso o utilizzando una soluzione salina. Alcuni autori suggeriscono l’iniezione preliminare di una soluzione di Tecnezio-99m rilevabile mediante gamma camera.
Pratiche cliniche per la gestione dello stravaso dei radiofarmaci
La documentazione scientifica riguardante lo stravaso dei radiofarmaci è limitata, rendendo difficile definire precise raccomandazioni. Inoltre, la mancanza di dati accurati sulla prevalenza dei danni tissutali nei casi di stravaso non trattati complica la valutazione dell’efficacia dei trattamenti adottati. Si stima che circa un terzo degli stravasi di radiofarmaci vescicanti non trattati porti a ulcere e necrosi.
La European Association of Nuclear Medicine (EANM) consiglia, per il radiofarmaco terapeutico ibritumomab tiuxetano marcato con Yttrio-90, di intraprendere azioni come l’ipertermia locale, l’elevazione dell’estremità e il massaggio delicato per favorire il drenaggio linfatico e ridurre la dose locale di radiazioni. Analoghe indicazioni sono fornite nella linea guida EANM sul Radio-223, che suggerisce anche la misura della radioattività nella sede dello stravaso attraverso l’acquisizione di immagini ripetute per calcolare la dose assorbita e prevedere gli effetti avversi.
Altre linee guida della EANM e della Society of Nuclear Medicine and Molecular Imaging (SNMMI) focalizzate sulla terapia con radionuclidi non promuovono particolari consigli pratici in caso di stravaso, indipendentemente dalle potenziali complicazioni.
La pratica clinica generale per la gestione dello stravaso di radiofarmaci, nel rispetto delle norme igieniche e di radioprotezione, mira a limitare la quantità di radiofarmaco che diffonde nello spazio sottocutaneo o perivascolare.
Pratiche cliniche specifiche dovrebbero essere avviate solo su istruzione del medico nucleare in caso di stravaso di radiofarmaci:
- uso diagnostico: il rischio principale è la difficoltà o impossibilità di interpretare le immagini;
- radiotossicità moderata: radionuclidi come 201Tl e 67Ga possono causare lesioni al punto di iniezione a seconda della dose stravasata.
- uso terapeutico: le azioni da intraprendere sono simili alla terapia decongestionante completa usata per il trattamento del linfedema, includendo opzioni come il debulking chirurgico e la ricostruzione microchirurgica.
In caso di febbre e dolore locale rilevante, si dovrebbe preferire un approccio con copertura antibiotica e terapia con eparina antitrombotica. Un’altra opzione per ridurre gli effetti dello stravaso è la tecnica di aspirazione-lavaggio, utilizzata dai chirurghi per le chemioterapie vescicanti, che deve essere messa in atto entro sei ore.
Un’ulteriore pratica clinica in uso presso il Maastricht University Medical Center merita valutazione. Anche per lo stravaso di radiofarmaci diagnostici, in caso di sintomi rilevanti, si raccomanda il consulto del chirurgo plastico. Fino alla decisione per l’intervento chirurgico, l’area infiltrata viene raffreddata per impedire la diffusione del radiofarmaco nei tessuti circostanti. Se non si opta per l’intervento chirurgico, si raccomanda di riscaldare frequentemente l’area di stravaso e di elevare il braccio per promuovere la diffusione del radiofarmaco.
La natura radioattiva dei radiofarmaci può essere sfruttata per l’imaging dell’area stravasata, aiutando a rilevare e quantificare la quantità di radiofarmaco infiltrato nel tessuto circostante, cosa non possibile per i farmaci chemioterapici tradizionali.
Conseguenze dello stravaso di radiofarmaci

Lo stravaso di radiofarmaci diagnostici può causare danni diretti al paziente, come necrosi cutanea o sindrome compartimentale. Tuttavia, la conseguenza più comune è una modifica della biodistribuzione del farmaco, che comporta un rischio significativo di interpretazione errata dell’esame e del conseguente inquadramento diagnostico.
Un dettaglio relativo ai danni da radiazioni in funzione della dose assorbita è riportato nella Guida Pratica pubblicata dalla Società Francese di Radioprotezione.
| Danno | Ritardo di apparizione dei sintomi (giorni) | Dose d’irradiazione (Gy) |
|---|---|---|
| Alopecia e perdita di peli | 17-21 | 3 |
| Eritema | 17-21 | 4-8 |
| Desquamazione secca | 17-28 | 8-15 |
| Desquamazione umida (piccolo flittene) | 17-45 | 15-20 |
| Desquamazione umida (grande flittene) | 17-45 | 20-25 |
| Necrosi | Diversi mesi | >25 |
Dall’analisi della letteratura disponibile, i danni tissutali causati da radiazioni appaiono rari, seppur non completamente assenti, e si presentano sotto forma di ulcere a esordio tardivo o lesioni pruriginose ed eritematose.
Indipendentemente dal tipo di radiofarmaco somministrato (diagnostico o terapeutico), il sintomo più frequente in caso di stravaso è l’eritema, associato o meno a prurito, che potrebbe richiedere l’applicazione di corticosteroidi.
Lo stravaso di radiofarmaci terapeutici
I seguenti casi riportano esempi di stravaso di radiofarmaci marcati con Ittrio-90, Lutezio-177 e Radio-223, le cui dosi assorbite possono variare da pochi Gy a oltre un centinaio di Gy.
Nei casi clinici pubblicati, i pazienti hanno avvertito un’immediata sensazione di dolore bruciante, eritema ed edema in seguito allo stravaso di Stronzio-89 e Ittrio-90-ibritumomab. Kawabe e colleghi hanno discusso le linee guida di sicurezza per lo stravaso di Stronzio-89, che includono quattro passaggi:
- documentare il sito con una fotografia;
- riscaldare la regione per promuovere la vasodilatazione e alleviare il dolore;
- considerare l’uso di steroidi topici o intralesionali;
- effettuare imaging dell’area per misurare la dose di radiazioni assorbite dalla pelle.
Un caso clinico documenta lo stravaso di Radio-223 cloruro somministrato nella regione dorsale della mano sinistra, che ha causato dolore locale, eritema ed edema. Quattro mesi dopo, nel sito di iniezione è stata diagnosticata una lesione a rapida crescita, rivelatasi un carcinoma cutaneo squamoso. Gli autori raccomandano che i pazienti con stravaso di radioterapie endovenose siano monitorati da un dermatologo per lo sviluppo di possibili tumori cutanei aggressivi.
Terwinghe et al. hanno implementato una pratica clinica per uno stravaso di [90Y]Y-DOTATOC, basata su:
- lavaggio rapido dei tessuti;
- elevazione del braccio per aumentare il flusso sanguigno;
- riscaldamento per accelerare la vasodilatazione;
- attivazione muscolare dell’area infiltrata.
Queste misure hanno dato ottimi risultati durante il follow-up, grazie al peso molecolare relativamente basso del radiofarmaco, che facilita il rapido allontanamento dai tessuti rispetto a radiofarmaci con peso molecolare più elevato, come [90Y]Y-ibritumomab tiuxetano.
Disposizioni simili sono presenti nelle linee guida tedesche di PRRT per il radiofarmaco [177Lu]-DOTATATE e sono state adottate da Schlenkhoff et al. anche per il radiofarmaco [177Lu]-PSMA-617, con buoni risultati in termini di efficacia.
Ladrière et al. sottolineano l’importanza della stima preliminare della distribuzione della dose nell’area dello stravaso e della comunicazione dell’evento al medico nucleare, al fisico medico e al radiofarmacista. La dose assorbita può essere determinata mediante imaging SPECT/CT immediatamente dopo lo stravaso, con scansioni di follow-up al giorno 5 e al giorno 7.
Aspetti legali sulla gestione dello stravaso
Il fenomeno dello stravaso rientra nella cosiddetta Nursing Malpractice, che comprende “gli errori derivanti da inadeguatezza, incapacità, imperizia a fornire prestazioni professionali con la destrezza generalmente esigibile da un professionista e che si concretizza in un danno o lesione al paziente”. Questo fenomeno assume risvolti non solo clinici, ma anche legali, coinvolgendo la responsabilità dell’operatore, soprattutto se non viene individuato per tempo o se l’ospedale non è dotato di un protocollo specifico. Tale circostanza può determinare una responsabilità a catena anche per altri operatori sanitari.
In sanità, il profilo di rischio è caratterizzato dal rischio clinico, definito come “la probabilità che un paziente sia vittima di un evento avverso imputabile alle cure mediche prestategli durante il periodo di degenza, in grado di causare un prolungamento dello stesso, un peggioramento delle condizioni di salute o la morte”. Secondo le linee guida emanate dal Ministero della Salute in tema di “Sicurezza dei pazienti e gestione del rischio clinico”, la fase di educazione è cruciale nel percorso formativo dell’operatore sanitario. In particolare, per i pazienti oncologici, essa deve essere focalizzata sul riconoscimento precoce dello stravaso.
Una recente “Linea guida sulla prevenzione degli errori connessi alla errata gestione di radiofarmaci” raccomanda la presenza di una procedura per la gestione dello stravaso tra gli elementi utili a mitigare il rischio clinico connesso alla somministrazione di radiofarmaci.
Conclusioni
Raramente vengono segnalate conseguenze a lungo termine dovute allo stravaso di radioisotopi per via endovenosa con lesioni da radiazioni. Tuttavia, con l’aumento dell’uso di isotopi radioattivi a scopi terapeutici, le informazioni riguardanti la prevenzione, il trattamento e il monitoraggio a lungo termine del sospetto danno da stravaso diventeranno sempre più importanti.
Le informazioni relative all’insorgenza, alla prevalenza e all’impatto degli stravasi rimangono fortemente limitate, anche se vi è una chiara tendenza all’aumento del numero di pubblicazioni. Questo aumento è potenzialmente correlato a una maggiore consapevolezza e interesse per l’argomento. Di particolare rilievo è l’aumento delle revisioni della letteratura e delle analisi di popolazioni di pazienti più ampie, che consentono una valutazione più globale dei problemi legati allo stravaso di radiofarmaci. Una maggiore segnalazione attraverso pubblicazioni è fondamentale per comprendere il reale impatto degli stravasi sia per i radiofarmaci diagnostici che terapeutici.
Esiste un’asimmetria informativa tra operatore sanitario e paziente, che potrebbe essere mitigata attraverso l’implementazione di alcuni strumenti, quali:
- consenso informato sullo stravaso: permette all’operatore sanitario di ottenere i dati utili per una corretta elaborazione dell’anamnesi e della cura, e al paziente di acquisire le informazioni necessarie al trattamento, potendo aderire in modo libero e autonomo, o rifiutarlo consapevolmente;
- opuscoli informativi per pazienti: favoriscono e migliorano la comunicazione medico-paziente, aiutando il medico a trasferire utili informazioni al paziente;
- foglio di dichiarazione dello stravaso da radiofarmaco: garantisce la tracciabilità dell’incidente, da riportare e conservare nella cartella del paziente (cartacea e/o informatica) e nel reparto.
Ad oggi non sono state pubblicate linee guida, procedure o raccomandazioni per la gestione dello stravaso di radiofarmaci. Sarebbe auspicabile proporre la creazione di un gruppo di lavoro multidisciplinare, come già istituito dalla Società Francese dei Radiofarmaci (SoFRa), che si impegni a sviluppare un protocollo clinico adeguato. In questo ambito, l’Area Radiofarmacia SIFO, che da sempre si impegna a portare avanti in maniera multidisciplinare tematiche importanti nel settore dei radiofarmaci, si propone per svolgere un ruolo attivo sia nel promuovere una cultura di gestione di ogni evento avverso sia nella redazione di un protocollo nazionale sullo stravaso dei radiofarmaci.






