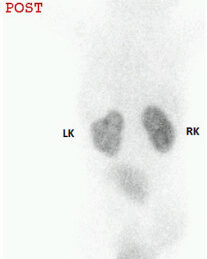
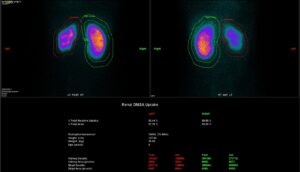
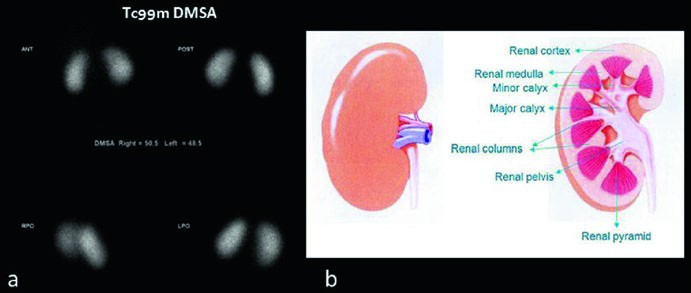
La scintigrafia renale statica con DMSA è una procedura in medicina nucleare basata sulla somministrazione per via endovenosa di un radiofarmaco (in questo caso il DMSA). Tale tracciante, una volta immesso nel circolo sanguigno, viene captato ed eliminato dai reni in modo proporzionale alla funzionalità renale. Può essere considerata il metodo di riferimento per la rilevazione di danni parenchimali focali.
La scintigrafia rileva il doppio dei difetti rispetto all’ecografia e quattro volte più difetti rispetto all’urografia endovenosa. Ha una sensibilità e specificità simili alla TC, con un’esposizione alle radiazioni inferiore e senza il rischio di reazioni al contrasto. Può anche fornire informazioni sulle dimensioni generali dei reni. Tuttavia, non fornisce informazioni dettagliate sul sistema collettore.
Indicazioni
La metodica è indicata per:
- valutare il danno parenchimale renale in varie nefropatie e studiare la funzionalità renale separata;
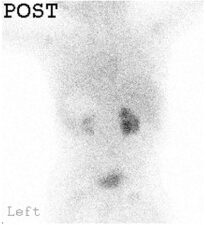
- sospetto di agenesia renale o di rene ectopico;
- caratterizzare di anomalie strutturali (rene a ferro di cavallo, displasie renali);
- valutare masse occupanti spazio (neoformazioni). Queste possono essere rilevate dall’imaging funzionale come difetti parenchimali. L’ecografia, la TC e la RM sono più adatte e dovrebbero essere raccomandate quando vengono rilevati difetti regionali nel parenchima. L’imaging funzionale può svolgere un ruolo prima degli interventi chirurgici per prevedere la funzione renale residua dopo la nefrectomia unilaterale parziale o completa;
- valutare parenchima residuo (reni policistici, insufficienza renale cronica);
- pielonefriti (diagnosi di pielonefrite acuta in pazienti con infezione delle vie urinarie, valutazione esiti cicatriziali, follow-up della pielonefrite).
Episodi successivi di pielonefrite acuta, se non diagnosticati o trattati adeguatamente, causano lo sviluppo di diverse cicatrici nel parenchima renale che portano ad una riduzione complessiva delle dimensioni del rene e ad una parallela riduzione della massa renale funzionale. I deficit della funzione corticale renale riscontrati nella pielonefrite acuta possono essere recuperati senza cicatrici se l’infezione viene individuata precocemente e trattata in modo appropriato.
La scansione deve essere eseguita durante o entro 2 settimane dall’episodio di infezione acuta.
L’intervallo di tempo minimo è di circa 6 mesi dall’infezione acuta per considerare i difetti corticali come cicatrici renali permanenti; - valutare danno parenchimale post-traumatico;
- valutare pre-chirurgicamente la funzionalità renale separata.
Radiotraccianti
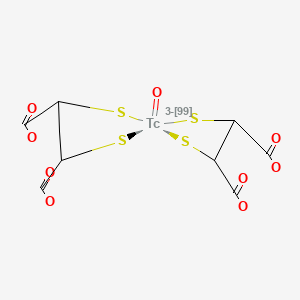
I radiotraccianti utilizzati si legano a livello corticale.
L’EANM ha individuato l’acido 99mTc-dimercaptosuccinico (DMSA) come miglior agente di imaging per visualizzare il coinvolgimento parenchimale renale. L’alternativa è il 99mTc-GH (99mTc-glucoeptonato).
Il 99mTc-DMSA e il 99mTc-GH (99mTc-glucoeptonato) si legano principalmente al tubulo prossimale della corteccia renale per un tempo prolungato dopo l’iniezione, per cui l’imaging tra le 4 e le 24 ore dopo la somministrazione del radiofarmaco mostra principalmente captazione corticale, senza interferenze da attività nel sistema escretore.
Il 99mTc-DMSA è preferito per la sua più alta ritenzione nel parenchima renale (30% vs 5-10% del GH). Un altro importante svantaggio del [99mTc] Tc-GH è il possibile accumulo e la stasi dell’attività nel sistema collettore, in particolare nel rene idronefrotico. Ciò può limitare la visualizzazione della corteccia renale e la valutazione accurata della funzione differenziale.
Il 99mTc-DMSA viene eliminato dal sangue mediante filtrazione glomerulare e secrezione tubulare; tuttavia, un’ampia frazione del tracciante filtrato viene riassorbita e trattenuta nelle cellule tubulari prossimali tubulare (corteccia renale), consentendo così di ottenere immagini ad alta risoluzione e ad alto contrasto.
Inizialmente si distribuisce nel fluido extracellulare, con una temporanea ritenzione nel fegato e milza. Circa il 90% del radiofarmaco circola nel sangue legato alle proteine plasmatiche.
L’estrazione renale è del 5% ad ogni passaggio e, a 1 ora dall’iniezione, circa il 50% dell’attività somministrata è trattenuta nelle cellule tubulari renali prossimali.
Now loading…
Preparazione e acquisizione
Non è richiesta una preparazione specifica del paziente. E’ importante una buona idratazione. A questo scopo è utile invitare il paziente a bere 500 ml di liquidi prima e dopo l’esame e di svuotare spesso la vescica per ridurre l’esposizione alle radiazioni della vescica e del bacino. Questo è particolarmente importante nei pazienti pediatrici. Raramente, potrebbe essere necessaria la sedazione dei bambini per evitare movimenti durante l’acquisizione. In questo caso dovrebbero essere istruiti a digiunare per 4-6 ore prima dell’esame.
Si somministra il radiofarmaco 99mTc-DMSA (Acido dimercaptosuccinico) per via endovenosa, tipicamente 1 MBq/kg di peso corporeo (Attività minima 18.5 MBq in età pediatrica, attività massima 160 Mbq (AIMN), 111 MBq EANM).
Dopo 2-4 ore dall’iniezione endovenosa di Tc-99m DMSA, al paziente viene chiesto di svuotare la vescica e di posizionarsi supino sul lettino. L’acquisizione si effettua con collimatore per le basse energie a fori paralleli ad alta risoluzione ed almeno 500k conteggi (Matrice: 128 x 128 o 256×256; Energia: 140 keV ± 10%).
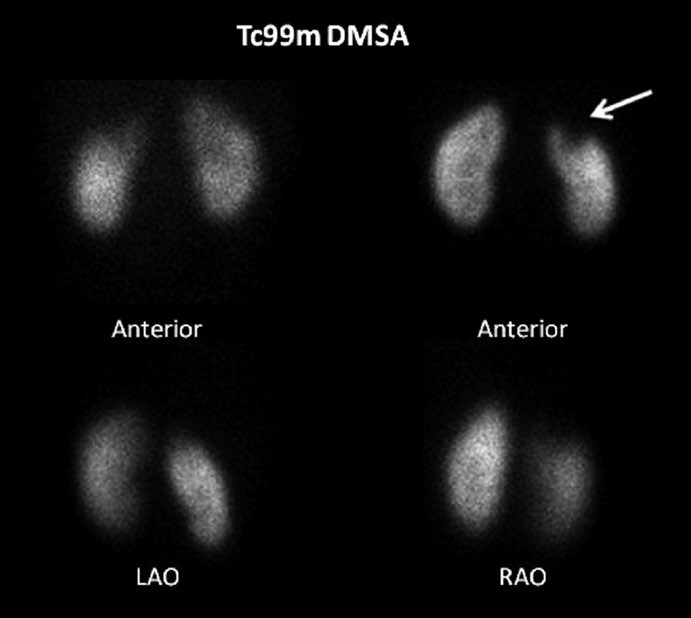
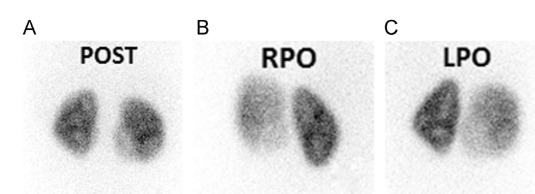
Abitualmente si effettuano proiezioni posteriore, obliqua-posteriore sinistra 45° ed obliqua-posteriore destra 45°.
In caso di rene ectopico, trapiantato o altre anomalie strutturali (ferro di cavallo etc.) si effettuano proiezione anteriore e posteriore al fine di calcolare la funzionalità renale percentuale di ciascun rene, con il calcolo della media geometrica di entrambe le proiezioni.
In rari casi, la presenza di reflusso vescico-ureterale, o di attività urinaria nel sistema collettore, può interferire con il calcolo della funzione renale differenziale (pelvi significativamente dilatate in ostruzioni, vescica neuropatica). In questi casi è possibile effettuare immagini tardive fino a 24 ore dall’iniezione. E’ inoltre possibile impiegare lo stimolo diuretico precedentemente alle immagini tardive o cateterizzazione (pratiche non comuni) per facilitare la fuoriuscita di urina radioattiva.
L’acquisizione SPECT è un’alternativa e viene eseguita se il paziente riesce a rimanere immobile durante l’acquisizione. Può essere utile per il rilevamento di piccoli difetti, specie quelli profondi all’interno del parenchima renale o per i pazienti con reni ectopici o trapiantati, per i quali le strutture ossee, l’intestino sovrapposto e la distanza paziente-detector possono rendere difficile la valutazione del profilo renale.
Non c’è consenso sulla sua utilità. La SPECT non è utilizzata di routine nei bambini a causa dell’aumento del tempo di imaging richiesto e del significato clinico non chiaro di piccoli difetti corticali aggiuntivi.
Elaborazione
Ai fini dell’indagine è importante la misurazione del diametro longitudinale renale alle immagini antero/posteriori.
Sull’immagine ottenuta in proiezione posteriore sono disegnate le regioni di interesse (ROI) renali utili al calcolo della funzionalità renale separata percentuale (basata sul confronto dei conteggi delle ROI renali)
In caso di proiezione anteriore e posteriore e possibile calcolare la media geometrica (maggiore affidabilità poiché tiene conto della profondità renale).
Si effettua quindi un’analisi semiquantitativa con il calcolo dell’indice di captazione di ciascun rene, espressione della capacità funzionale separata: i valori normali di funzionalità separata sono compresi fra 50%-50% e 45%-55%.
NB: Anche in caso di funzione renale ridotta bilateralmente tali valori possono risultare nel range di normalità.
L’indice è più affidabile nel caso si calcoli la media geometrica e meno affidabile in caso di IRC (per l’elevato background).
Now loading…
Interpretazione
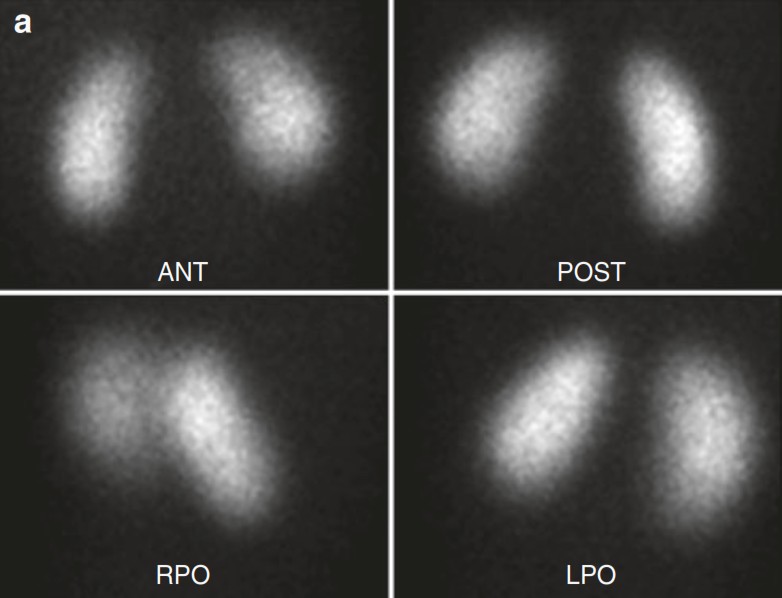
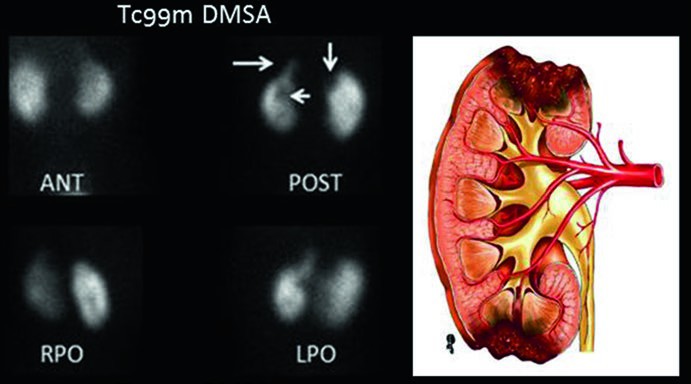
Nelle immagini normali si deve avere una diffusa e omogenea fissazione a livello della corticale renale (il DMSA non si fissa nella midollare e non deve trovarsi nel sistema escretore).
Il semplice appiattimento di un profilo, specie di quello superiore del rene sinistro (impronta splenica) o laterale (nei bambini piccoli con reni di forma triangolare), non è indicativo di lesione parenchimale.
Sono possibili ipoattività apparenti dei poli, specie di quelli superiori, per contrasto con le adiacenti colonne del Bertin ed in caso di atteggiamento ipertrofico/vicariante.
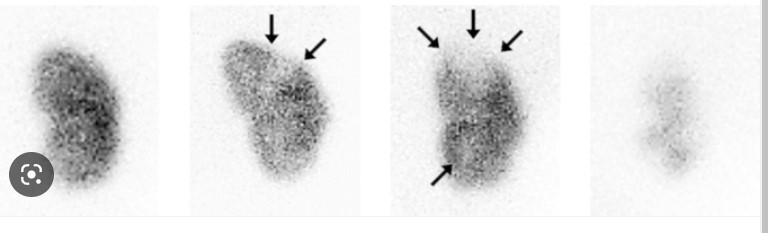
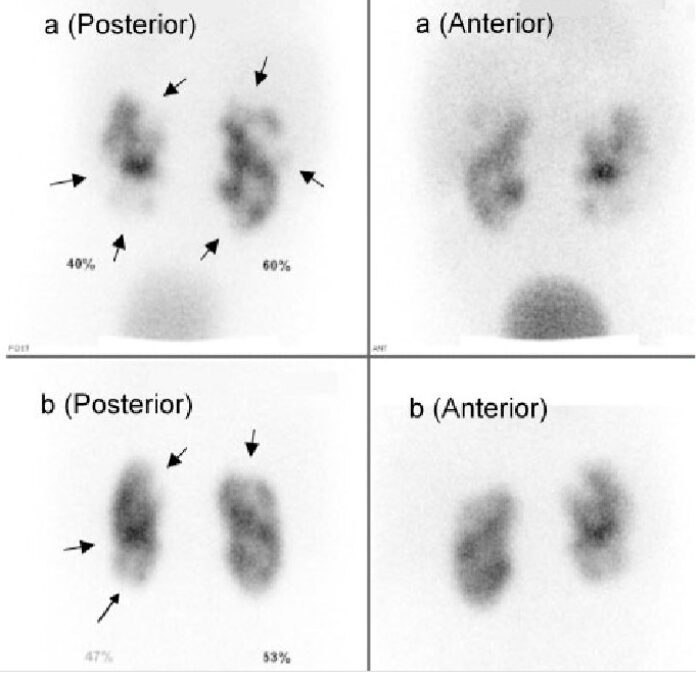
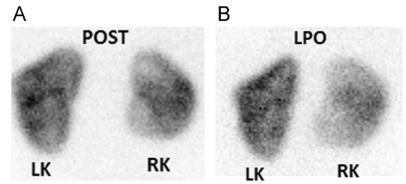
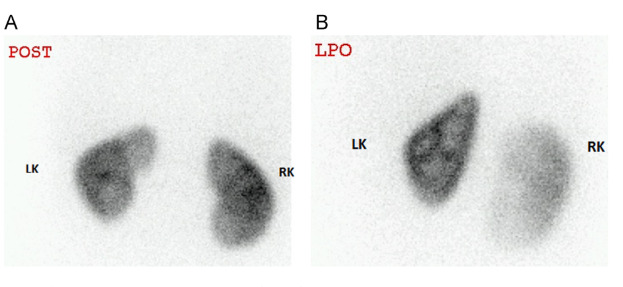
In caso di esiti cicatriziali è possibile vedere aree di ipofissazione con margini relativamente ben definiti, perdita di volume parenchimale e retrazione focale del contorno renale.
Morfologicamente si presenta come un difetto più comunemente a forma di cuneo, ovoidale o, in alternativa, un assottigliamento corticale, o un un appiattimento del contorno renale.
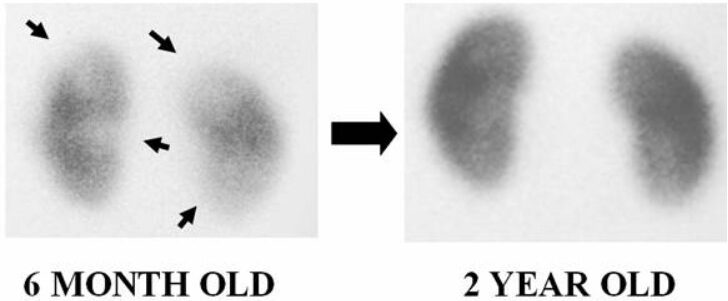
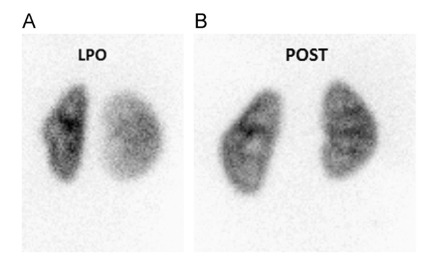
Nei soggetti con pielonefrite acuta si possono osservare difetti focali singoli o multipli. Si ha fissazione ridotta o assente del tracciante, margini indistinti e assenza di deformità di retrazione del contorno renale.

La distinzione tra pielonefrite acuta destinata a migliorare/guarire e cicatrici permanenti non è possibile con sicurezza anche se in genere un’area ipointensa più ampia, polare, che non deforma i contorni renali e ha margini indistinti rappresenta più probabilmente un’infezione acuta destinata a guarire. Infatti nella pielonefrite acuta, i difetti corticali appaiono più estesi rispetto alla fase cronica, a causa dell’edema e dell’ischemia associati ai focolai di infezione acuta. Se è presente deformazione localizzata del contorno renale e/o perdita di volume è più probabile che rappresenti una cicatrice permanente.
Tuttavia, solo il follow-up consente di distinguere tra lesioni acute e croniche; un difetto che persiste per più di 6 mesi è classificato come lesione cronica o cicatrice.
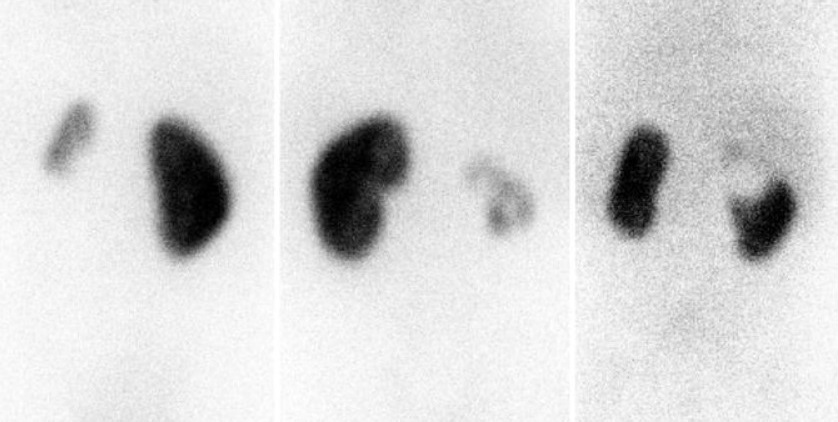
Nel caso di displasia renale, il rene appare asimmetricamente più piccolo e la captazione è ridotta o assente. La captazione, se presente, è per lo più eterogenea in tutto il rene o in una porzione del rene (nella displasia focale o segmentaria) senza un difetto periferico del contorno renale.
I reni displasici sono più inclini alle infezioni e alle cicatrici, per cui è possibile che le due condizioni coesistano. Occorre comunque ricordare che l’ecografia è la modalità preferita per valutare le anomalie morfologiche. La scintigrafia è utile soprattutto per valutare la funzione differenziale e per valutare eventuali cicatrici nel rene controlaterale.
Errori di interpretazione
Le immagini acquisite durante la scintigrafia renale statica molte volte possono essere interpretate in modo sbagliato o ci possono essere delle condizioni che possono provocare errori.
Contorni renali sfocati o doppi rappresentano generalmente movimenti del paziente.
Le aree di ipofissazione possono essere correlate anche ad altre alterazioni anatomiche (cisti, esiti ischemici, nodulazioni/masse, nel bambino presenza di lobulazioni fetali), per questo motivo è utile avere un imaging morfologico (ecografia o TC) da correlare.
In caso di cisti l’area ipoattiva è circondata da tessuto parenchimale funzionante, o nel caso sia marginale, è di aspetto più rotondeggiante.
Un rene ruotato può apparire come un rene “sottile” con un asse trasversale corto nella vista posteriore (utile osservare immagini oblique e eventualmente anteriori)
Un’area lineare di assente captazione del tracciante (setto inter-renicolare) che si estende dall’ilo renale al parenchima è visibile alla SPECT e può essere confusa con una cicatrice.
Esempi di varianti normali:
Referto
Per redirigere un adeguato referto bisogna:
- descrivere i due reni separatamente con sede, dimensioni e morfologia;
- distribuzione del radiotracciante (omogenea, disomogenea);
- morfologia, numero e sede delle aree di ipofissazione, compresi eventuali retrazioni o irregolarità del profilo della corticale renale;
- significato visivo (impronta caliceale e assottigliamento corticale, esiti cicatriziali o significato aspecifico etc.).
Fonti:
- Fondamenti di medicina nucleare. Tecniche e applicazioni;
- Nuclear Medicine Companion: A Case-Based Practical Reference for Daily Use.
Fonte: A Concise Guide to Nuclear Medicine (Abdelhamid H. Elgazzar e Saud Alenezi)