La medicina nucleare costituisce un pilastro fondamentale nella diagnosi e nella gestione di numerose patologie cardiovascolari, offrendo strumenti di indagine non invasivi e estremamente precisi. Il suo contributo principale risiede nella capacità di valutare non solo l’anatomia, ma soprattutto la funzione del cuore, un aspetto spesso critico per la cura del paziente.
Caricamento…
L’esame cardine in questo campo è la scintigrafia miocardica di perfusione (MPI), uno degli studi più comunemente eseguiti. Questa tecnica permette di determinare con accuratezza l’adeguatezza del flusso sanguigno al muscolo cardiaco (miocardio). L’esame viene solitamente eseguito in concomitanza con uno stress, che può essere fisico (su cicloergometro o cyclette) o farmacologico, per individuare e valutare la presenza e la gravità di una malattia coronarica (CAD).
La scintigrafia di perfusione può essere condotta con diversi radioisotopi e protocolli. Il protocollo a isotopo singolo utilizza composti marcati con Tecnezio-99m (sestamibi o tetrofosmin), mentre quello a doppio isotopo combina il Tecnezio-99m con il Tallio-201.
Caricamento…
L’innovazione più significativa arriva però dalla Tomografia a Emissione di Positroni (PET), che impiega traccianti specifici. La PET cardiaca apporta un valore aggiunto straordinario, permettendo non solo una valutazione morfofunzionale più precisa della coronaropatia, ma anche una sua quantificazione oggettiva (ad esempio, calcolando la riserva di flusso coronarico – FFR). Inoltre, è l’unica metodica in grado di valutare il metabolismo del miocardio e determinarne la vitalità, distinguendo un tessuto sano da uno necrotico o ibernato, informazioni cruciali per decidere se un’area cardiaca può trarre beneficio da una rivascolarizzazione.
Oltre all’ambito coronarico, la medicina nucleare offre soluzioni diagnostiche preziose per altre condizioni, come la diagnosi certa di emangiomi dei tessuti molli e la valutazione del linfedema attraverso la linfoscintigrafia.
Indice:
- Valutazione della funzione cardiaca
- Valutazione della perfusione e del metabolismo miocardico
- Diagnosi di malattia coronarica
- Prognosi e stratificazione del rischio
- Follow-Up dopo un Infarto Miocardico Acuto
- Follow-Up dopo procedure di rivascolarizzazione
- Valutazione pre-operatoria
- Valutazione della vitalità miocardica
- Lo studio dell’emangioma dei tessuti molli
- La linfoscintigrafia
Valutazione della funzione cardiaca
Uno degli esami fondamentali per la valutazione non invasiva della funzione cardiaca è lo studio sincronizzato gated del blood pool cardiaco (o ventricolografia isotopica). Questo esame si effettua osservando il pool ematico intracardiaco marcando i globuli rossi con Tecnezio-99m.
Attraverso un elettrocardiogramma sincronizzato (gating), la telecamera gamma acquisisce immagini in movimento del cuore, suddivise per le diverse fasi del ciclo cardiaco. Questo permette di analizzare in modo dettagliato la cinetica regionale delle pareti cardiache e la sincronia della contrazione (asincronia). Inoltre, consente di misurare con elevata accuratezza e riproducibilità parametri emodinamici fondamentali, primo fra tutti la frazione di eiezione del ventricolo sinistro (LVEF), ma anche la funzione diastolica e i volumi ventricolari.
È importante notare che questo esame visualizza e valuta la cavità ventricolare e il movimento del sangue, ma non permette di osservare direttamente il muscolo cardiaco. Nonostante questo, rimane uno strumento clinico insostituibile in diverse situazioni, tra cui il monitoraggio della cardiotossità indotta da chemioterapici come la doxorubicina, il workup diagnostico dello scompenso cardiaco, la valutazione prognostica in seguito a un infarto miocardico acuto e la valutazione del rischio cardiaco pre-operatorio.
Valutazione della perfusione e del metabolismo miocardico
Le manifestazioni cliniche della malattia coronarica (CAD) sono varie e insidiose, spaziando dall’angina pectoris all’infarto miocardico, dallo scompenso cardiaco congestizio alla morte improvvisa. Spesso, la malattia progredisce in modo silente, senza sintomi evidenti, fino a quando non raggiunge uno stadio avanzato e potenzialmente pericoloso.
La maggior parte dei metodi diagnostici, sia invasivi come la coronarografia, sia non invasivi, si basa sul rilevamento di un restringimento del lume (lume) dei vasi coronarici epicardici. Tuttavia, c’è un aspetto fisiologico cruciale da considerare: un restringimento arterioso fino al 75% dell’area della sezione trasversa (che corrisponde a meno del 50% del diametro del lume) non altera il flusso sanguigno coronarico a riposo. Il problema emerge sotto sforzo, quando il cuore richiede più ossigeno.
È qui che entra in gioco il principio dello stress, cardine della scintigrafia miocardica di perfusione. L’aumento della richiesta di flusso coronarico, indotto da uno sforzo fisico (su cicloergometro) o da agenti farmacologici vasodilatatori (come adenosina o dipiridamolo) o stimolanti (come la dobutamina), esaspera le differenze di flusso tra le diverse regioni del cuore. Un’arteria sana si dilata e aumenta il flusso in modo appropriato; un’arteria stenotica non può farlo adeguatamente, creando una disparità di perfusione (ischemia) che è possibile visualizzare.
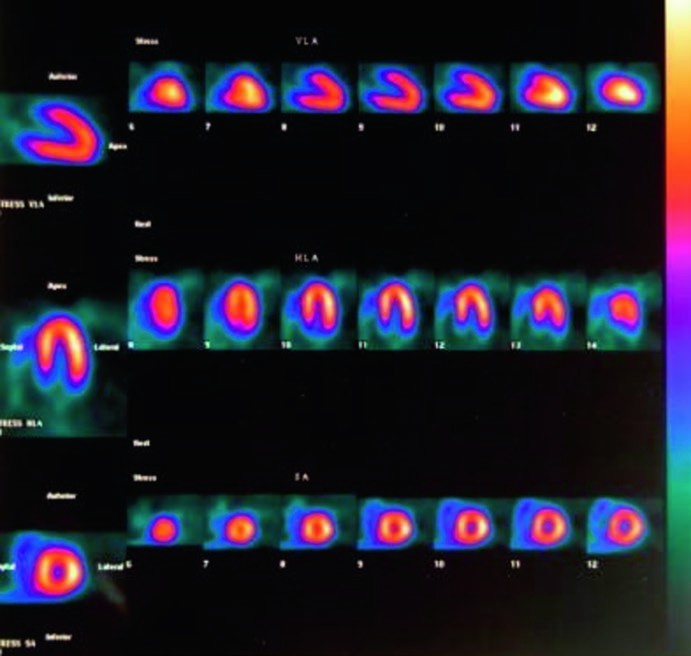
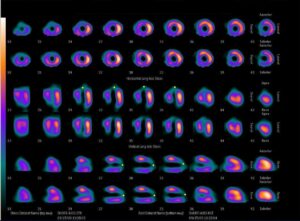
La scintigrafia di perfusione miocardica mappa proprio la distribuzione relativa del flusso sanguigno coronarico. In un cuore sano e senza pregresse cicatrici, questa distribuzione è uniforme. In presenza di una stenosi, l’immagine mostrerà una riduzione del tracciante in un’area specifica del muscolo cardiaco, la cui sede anatomica corrisponde al territorio di perfusione dell’arteria ristretta. L’entità del difetto di perfusione riflette la gravità cumulativa delle stenosi lungo l’albero coronarico e l’ampiezza del suo territorio a valle.
Pertanto, questo esame non si limita a una semplice diagnosi di presenza o assenza di malattia coronarica. Fornisce una valutazione completa dell’estensione, della gravità e dell’impatto fisiologico della malattia, offrendo un potere prognostico straordinario nel stratificare il rischio del paziente. Per questo motivo, la scintigrafia di perfusione è indicata in una vasta gamma di scenari clinici: dalla diagnosi di ischemia in pazienti con dolore toracico acuto o in diabetici (dove l’ischemia può essere “silente”), alla valutazione prognostica post-infarto, dal monitoraggio dell’efficacia di una rivascolarizzazione (bypass o angioplastica) alla valutazione del rischio pre-operatorio per interventi non cardiaci.
Diagnosi di malattia coronarica
La scintigrafia miocardica di perfusione (MPI) si conferma come uno strumento diagnostico estremamente affidabile. La letteratura scientifica riporta, per la diagnosi di malattia coronarica (CAD), valori medi di sensibilità vicina al 90% e di specificità attorno al 70-75%.
Il gold standard diagnostico rimane l’angiografia coronarica, una metodica invasiva che visualizza direttamente il lume delle arterie. Tuttavia, è importante riconoscere i limiti di questo stesso gold standard: l’angiografia tende a sottostimare sistematicamente l’estensione della malattia aterosclerotica diffusa (che non sempre causa stenosi focali severe) e non fornisce informazioni sulla reale rilevanza fisiologica di una stenosi sul flusso sanguigno (valutabile invece con la riserva di flusso coronarico: FFR).
Stabilire la reale accuratezza della MPI è complesso a causa di un bias metodologico noto come “post-test referral bias” o “verification bias“. In pratica, i pazienti con un risultato negativo alla scintigrafia raramente vengono inviati a eseguire un’angiografia coronarica, una scelta clinica più che giustificata data l’eccellente prognosi associata ad un esame di perfusione normale. Questa pratica, però, distorce le analisi retrospettive, poiché la popolazione che si sottopone all’angiografia (il gold standard) è già pre-selezionata per avere un’alta probabilità di malattia.
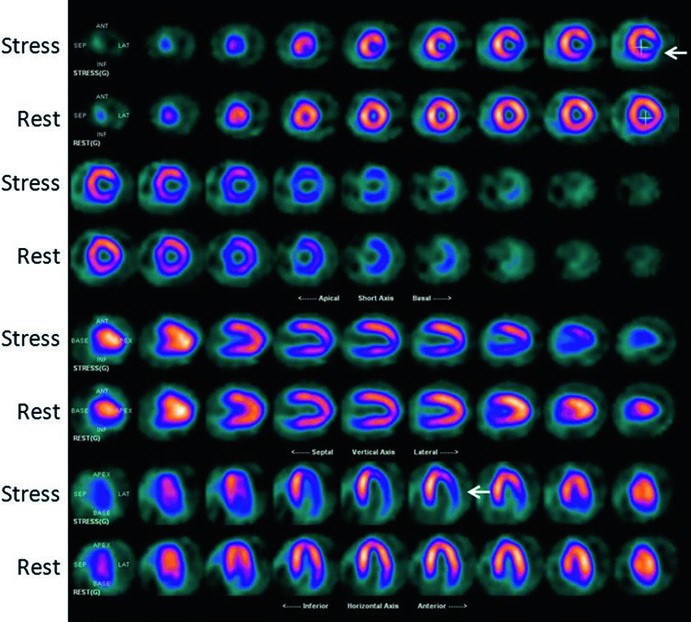
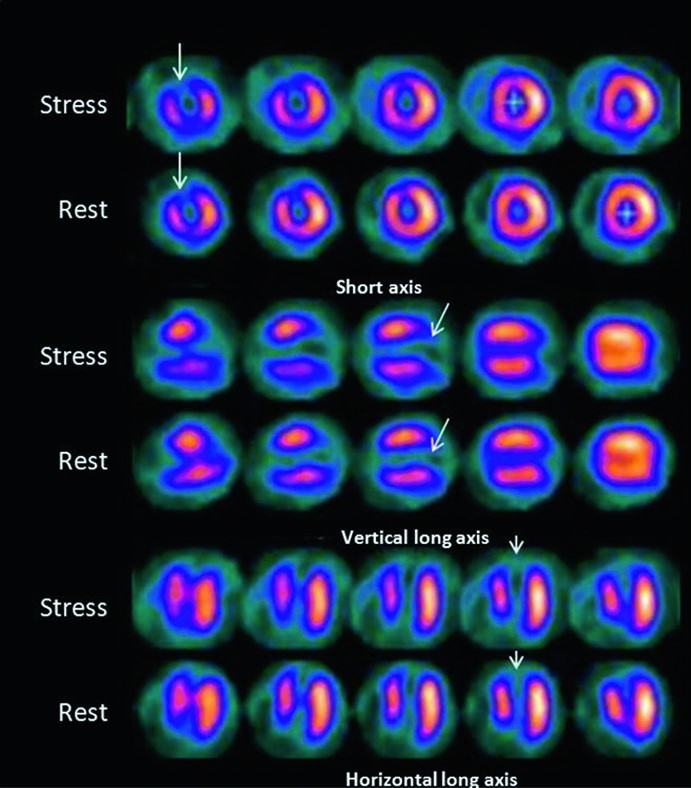
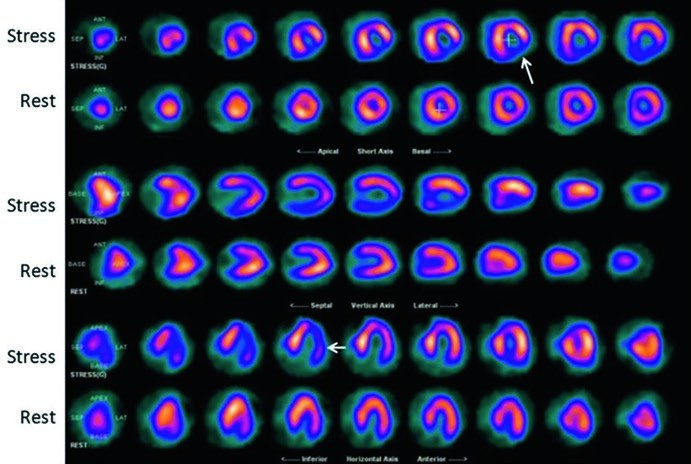
All’esame scintigrafico, l’ischemia miocardica si manifesta come un difetto di perfusione che compare o si accentua sotto sforzo e che migliora o scompare completamente alle immagini di riposo.
Questo pattern “reversibile” è il segno distintivo della presenza di una stenosi coronarica emodinamicamente significativa.
Caricamento…
Prognosi e stratificazione del rischio
Oltre alla diagnosi, il vero punto di forza della scintigrafia di perfusione è la sua straordinaria capacità di stratificare il rischio dei pazienti con CAD stabile, guidando le decisioni terapeutiche più appropriate.
L’esame fornisce un quadro multidimensionale della malattia:
- estensione e gravità: le alterazioni di perfusione vengono classificate in base alle dimensioni, alla sede, alla gravità e al grado di reversibilità (ischemia);
- funzione cardiaca: permette di quantificare parametri cruciali come i volumi ventricolari, l’ispessimento sistolico delle pareti, la cinetica segmentaria e la frazione di eiezione del ventricolo sinistro (LVEF). Anche la dimensione e la funzione del ventricolo destro possono essere valutate.
Un pattern di perfusione normale in un paziente che ha raggiunto un adeguato livello di stress è associato a una prognosi eccellente a breve termine, con un tasso di eventi cardiaci inferiore all’1% all’anno, indipendentemente dall’anatomia coronarica sottostante.
Al contrario, la presenza di anomalie nella perfusione definisce la prognosi. L’entità del danno è misurata dal numero di segmenti cardiaci coinvolti, dalla gravità dei difetti e dall’ampiezza dell’ischemia reversibile. Quando queste informazioni si integrano con i dati del test da sforzo (ad esempio, la capacità funzionale, l’insorgenza di alterazioni ECG) e con i parametri di funzione ventricolare, il valore prognostico combinato supera quello della sola angiografia coronarica.
I dati sono eloquenti: il tasso medio annuo di eventi cardiaci (morte o infarto) è dodici volte più alto nei pazienti con immagini anormali rispetto a quelli con immagini normali.
Sia i difetti fissi (indicativi di necrosi cicatriziale da pregresso infarto) che quelli reversibili (ischemia) hanno un significato prognostico, ma predicono outcome diversi: i difetti fissi sono un predittore di morte cardiaca, mentre i difetti reversibili sono un importante predittore di infarto miocardico non fatale.
Il rischio è tanto maggiore quanto più severe sono le anomalie riscontrate.
Follow-Up dopo un Infarto Miocardico Acuto
Dopo un evento acuto come un infarto miocardico, la scintigrafia di perfusione eseguita in fase precoce o prima della dimissione ospedaliera assolve a due compiti fondamentali per la gestione successiva del paziente. Il primo è valutare con precisione l’entità del danno miocardico sostenuto, quantificando la massa di tessuto necrotico e cicatriziale e determinando il suo impatto sulla funzione cardiaca globale, in particolare attraverso la misurazione della frazione di eiezione ventricolare sinistra. Il secondo, altrettanto cruciale, è identificare la presenza di ischemia residua in territori diversi da quello colpito dall’infarto. La rilevazione di ischemia residua indica che persistono altre stenosi coronariche critiche non trattate, le quali comportano un rischio elevato di nuovi eventi ischemici, guidando così la decisione di procedere con ulteriori accertamenti come l’angiografia e potenziali rivascolarizzazioni.
Follow-Up dopo procedure di rivascolarizzazione
Dopo un intervento di rivascolarizzazione coronarica, sia essa un’angioplastica percutanea (PCI) con impianto di stent o un intervento di bypass chirurgico (CABG), esiste il rischio concreto di restenosi (restringimento) all’interno dello stent o di occlusione dei graft venosi o arteriosi. Molto spesso, questi eventi sono asintomatici o si presentano con sintomi poco chiari. La scintigrafia di perfusione miocardica si rivela quindi uno strumento di monitoraggio efficiente e non invasivo, in grado di valutare l’effettiva efficacia dell’intervento nel ripristinare un flusso sanguigno adeguato. Un risultato negativo fornisce rassicurazione, mentre la scoperta di nuovi difetti di perfusione o la ricomparsa di ischemia in un territorio trattato identifica i pazienti che necessitano di una rivalutazione angiografica e di eventuali interventi aggiuntivi.
Valutazione pre-operatoria
La valutazione del rischio cardiologico pre-operatoria è fortemente raccomandata per i pazienti che, pur dovendo sottoporsi a interventi chirurgici non cardiaci, presentano fattori di rischio o sintomi suggestivi di malattia coronarica.
La decisione di eseguire uno studio di perfusione si basa su un’attenta analisi di diversi elementi: la presenza e la stabilità di una cardiopatia nota, condizioni concomitanti come il diabete mellito (noto fattore di rischio per ischemia silente), la malattia vascolare periferica, l’insufficienza renale o polmonare, l’urgenza dell’intervento chirurgico (d’emergenza o elettivo) e il tipo di chirurgia programmata (con rischio cardiovascolare più o meno elevato).
Una stratificazione del rischio basata su test oggettivi come la MPI permette al medico e al paziente di scegliere consapevolmente il momento e le modalità migliori per l’intervento, ottimizzando le cure perioperatorie e la gestione terapeutica a lungo termine.
Valutazione della vitalità miocardica
Un’applicazione di cruciale importanza è la valutazione della vitalità miocardica. Esistono infatti aree di miocardio che appaiono ipocinetiche o acinetiche all’ecografia e perfuse scarsamente a riposo, ma che sono ancora vitali (ibernate). Queste cellule, pur essendo ipossiche e “addormentate”, possono recuperare la loro funzione se viene ripristinato un adeguato afflusso di sangue.
Caricamento…
Nei pazienti con coronaropatia e disfunzione ventricolare severa, distinguere un miocardio vitale ma ipoperfuso (ibernato) da un miocardio necrotico e cicatriziale è una delle decisioni più critiche. Questa distinzione determina l’intero corso della gestione terapeutica: la rivascolarizzazione è giustificata e potenzialmente benefica solo se è presente una quantità significativa di miocardio vitale recuperabile.
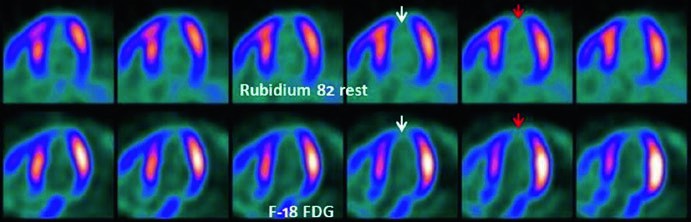
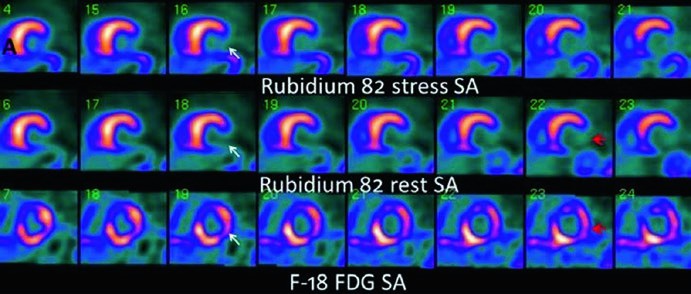
Sebbene il tallio-201 in protocolli specifici possa essere utilizzato, il gold standard non invasivo per la valutazione della vitalità è la Tomografia a Emissione di Positroni (PET) con F-18-FDG. Questo esame valuta il metabolismo glucidico del miocardio: un tessuto vitale, pur essendo ipoperfuso a riposo, mostra ancora un metabolismo attivo del glucosio (un fenomeno noto come “mismatch perfusione-metabolismo“), segno che le cellule sono ancora vive e possono riprendere a contrarsi se adeguatamente riperfuse. Al contrario, un tessuto necrotico non mostra né perfusione né metabolismo (“match perfusione-metabolismo”), indicando una cicatrice irreversibile.
Lo studio dell’emangioma dei tessuti molli
Gli emangiomi dei tessuti molli rappresentano la più comune lesione angiomatosa, costituendo circa il 7% di tutti i tumori benigni dei tessuti molli nella popolazione generale, con una prevalenza maggiore nel sesso femminile. Queste lesioni vascolari vengono classificate in cinque categorie principali in base al tipo di canale vascolare predominante: capillare, cavernoso, artero-venoso, venoso e forme miste.
La scintigrafia con globuli rossi marcati con Tecnezio-99m (Tc-99m) offre un approccio diagnostico non invasivo estremamente valido per la caratterizzazione di queste lesioni. La sua utilità principale risiede nella capacità di evitare biopsie non necessarie, procedure che in queste formazioni vascolari possono comportare un rischio significativo di complicanze emorragiche.
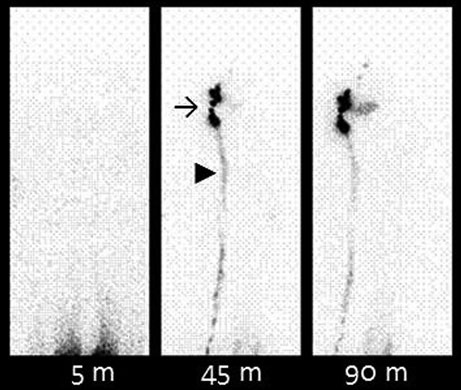
L’esame, eseguito con una tecnica di angiografia scintigrafica in tre fasi (flusso sanguigno, pool vascolare immediato e immagini tardive), permette di identificare il tipico “pooling” del tracciante all’interno delle lacune vascolari dell’emangioma. Lo scanning total-body con RBCs marcati è particolarmente utile per determinare la natura della lesione, valutarne l’estensione anatomica e identificarne la molteplicità in caso di malattia sistemica, fornendo una mappa completa della patologia.
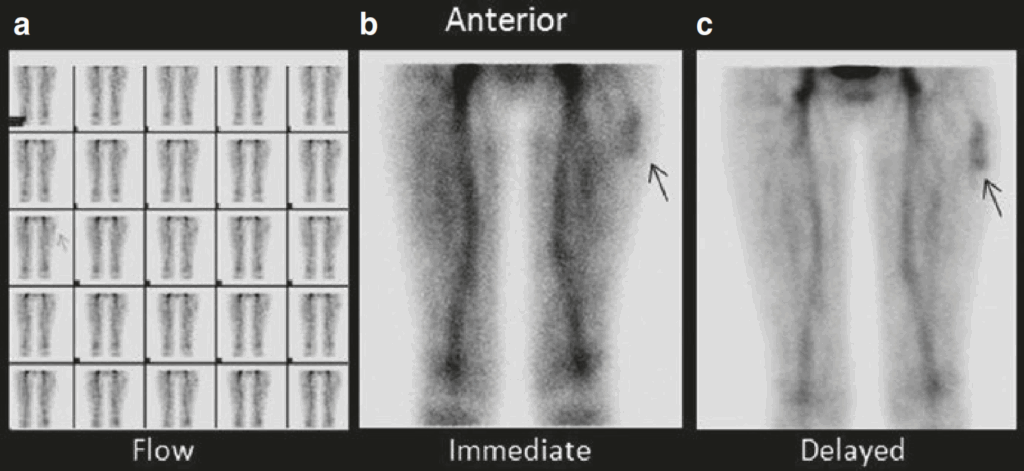
Le immagini di perfusione dinamica (a) mostrano un aumento del flusso nella regione superiore della coscia sinistra. Le immagini immediate (b) e tardive (c) in proiezione anteriore e posteriore delle cosce evidenziano un’attività aumentata del radiofarmaco nel terzo superiore della coscia (freccia). I reperti sono compatibili con un emangioma dei tessuti molli.
La linfoscintigrafia
La linfa è un fluido corporeo caratterizzato da un basso contenuto proteico, un alto livello di lipidi e la presenza di linfociti. Il suo drenaggio dai tessuti periferici avviene attraverso una rete di vasi linfatici che convogliano il liquido verso i linfonodi regionali per poi farlo confluire nel circolo venoso centrale. L’insufficienza di questo sistema di drenaggio in una specifica area del corpo porta all’accumulo di liquidi e allo sviluppo di linfedema.
La linfoscintigrafia è la metodica di elezione per studiare questo processo. La tecnica prevede l’iniezione intradermica di microparticole radio-markate (solitamente nanocolloidi di albumina marcati con Tc-99m) a livello degli spazi interdigitali delle mani o dei piedi. Il successivo follow-up mediante imaging scintigrafico permette di visualizzare in tempo reale il movimento del tracciante attraverso i collettori linfatici, misurandone la velocità di progressione e la funzionalità dei linfonodi.
Questo studio, affidabile, di facile esecuzione e ben tollerato dal paziente, è indicato per la diagnosi differenziale del linfedema, sia nelle forme primitive (da malformazione congenita del sistema linfatico) che in quelle secondarie, che rappresentano la causa più frequente e sono spesso conseguenza di interventi chirurgici (come la dissezione linfonodale ascellare nel carcinoma mammario) o di radioterapia.
Un segno scintigrafico di grande rilevanza, specialmente nello studio degli arti inferiori, è la presenza del “dermal backflow” (flusso retrogrado dermico). Questo fenomeno, insieme a un ridotto uptake nei linfonodi poplitei o inguinali, indica una severa alterazione funzionale del sistema linfatico, con riflusso del tracciante nel derma, ed è correlato a una maggiore gravità e una più lunga durata della disfunzione linfatica. La linfoscintigrafia fornisce dunque non solo una diagnosi ma anche preziose informazioni sulla stadiazione e l’entità del deficit.
Fonte: A Concise Guide to Nuclear Medicine (Abdelhamid H. Elgazzar e Saud Alenezi)