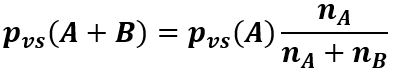Gli anestetici inalatori sono fondamentali nell’anestesia generale, apprezzati per la loro rapidità d’azione e il recupero veloce, caratteristiche che ne aumentano l’efficienza e la sicurezza. Tra questi, solo il protossido d’azoto (N₂O) è un gas vero e proprio; gli altri, spesso denominati “gas anestetici“, sono in realtà vapori di liquidi volatili che, sebbene liquidi a temperatura e pressione ambiente, vengono somministrati in fase gassosa attraverso i polmoni.
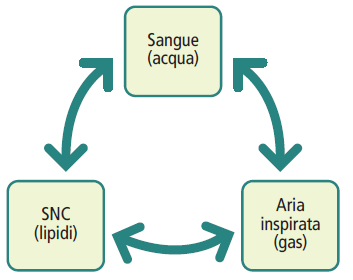
Dopo l’inalazione, il vapore anestetico viene assorbito a livello alveolare nel flusso sanguigno e si distribuisce nei vari tessuti, incluso il sistema nervoso centrale (SNC), l’organo target. Questo processo avviene secondo gradienti di concentrazione e pressione parziale, nonché in base alle specifiche proprietà chimico-fisiche di ciascun anestetico, fino al raggiungimento di uno stato di equilibrio. In tale stato, la pressione parziale dell’agente anestetico negli alveoli polmonari è uguale a quella nel sangue e nel SNC.
La solubilità degli anestetici nel sangue è determinante per la velocità di induzione e risveglio dell’anestesia. Il coefficiente di ripartizione sangue/gas indica l’idrosolubilità di un gas e rappresenta il rapporto, all’equilibrio, tra la concentrazione del gas in fase liquida e quella in fase gassosa. Un coefficiente più basso implica un’induzione e un risveglio più rapidi, poiché l’equilibrio tra la pressione parziale del gas anestetico negli alveoli e nel sangue viene raggiunto più velocemente. Ad esempio, anestetici poco solubili nel sangue come sevoflurano, desflurano e N₂O inducono rapidamente l’anestesia generale e consentono un risveglio altrettanto rapido rispetto a composti più solubili come l’alotano, ormai in disuso.
Il coefficiente di ripartizione olio/gas, indicativo della liposolubilità di un gas, rappresenta il rapporto all’equilibrio tra la concentrazione del farmaco in fase gassosa e quella in fase oleosa. Un anestetico altamente liposolubile tende ad essere più potente, data l’affinità per i tessuti, ma può anche accumularsi nel tessuto adiposo, prolungando il risveglio e aumentando il rischio di effetti collaterali.
Oltre ai coefficienti di ripartizione, altri fattori influenzano la rapidità di induzione e risveglio dell’anestesia inalatoria:
- concentrazione inspiratoria dell’anestetico: un aumento della concentrazione inspiratoria accelera l’induzione;
- ventilazione/minuto: un incremento della ventilazione/minuto favorisce un più rapido aumento della pressione parziale alveolare dell’anestetico;
- portata cardiaca: una riduzione della portata cardiaca diminuisce la distribuzione dell’anestetico nei tessuti periferici, consentendo un più rapido raggiungimento dell’equilibrio tra la pressione parziale alveolare e quella nel SNC.
Fasi dell’anestesia inalatoria:
- induzione: inizia la somministrazione dell’anestetico nella miscela respiratoria; la pressione parziale dell’anestetico negli alveoli sarà maggiore rispetto a quella nel sangue e nel SNC, guidando lo spostamento del gas dagli alveoli al sangue e al SNC fino al raggiungimento dell’equilibrio;
- mantenimento: Se la concentrazione alveolare dell’anestetico rimane costante, la sua pressione parziale sarà la stessa nel sangue e nel SNC, senza un gradiente di pressione parziale.
- risveglio: interrotta la somministrazione dell’anestetico, la sua pressione parziale alveolare sarà inferiore a quella nel sangue e nel SNC, creando un gradiente inverso che sposta il gas dal SNC al sangue e poi agli alveoli fino alla completa eliminazione.
Caricamento….
La principale via di eliminazione degli anestetici inalatori è quella polmonare, con una minima parte eliminata attraverso la cute e il metabolismo epatico.
La dose di vapore anestetico necessaria per ottenere l’effetto desiderato viene monitorata utilizzando la MAC (Minimum Alveolar Concentration). La MAC è la concentrazione alveolare di gas anestetico, espressa in percentuale di volume a un’atmosfera, che previene il movimento in risposta a uno stimolo chirurgico nel 50% dei pazienti. Più bassa è la MAC, maggiore è la potenza dell’anestetico inalatorio.
La MAC può essere influenzata da vari fattori:
- Riduzione della MAC: Somministrazione di oppioidi, benzodiazepine, età avanzata, gravidanza, anemia, ipotensione, ipotermia, acidosi metabolica.
- Aumento della MAC: Ipertermia, ipernatriemia, abuso cronico di alcol e variabilità genetica. Ad esempio, è stato osservato che le donne con capelli rossi presentano un aumento della MAC del 19%.
Anestetici alogenati: Sevoflurano e Desflurano
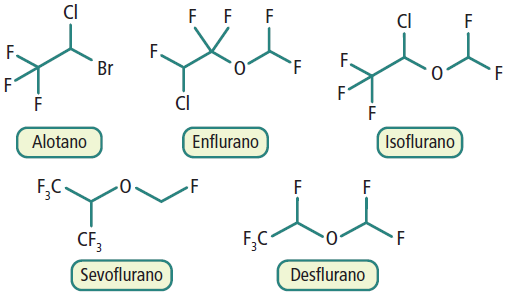
Gli anestetici alogenati sono eteri in cui gli atomi di idrogeno sono sostituiti da alogeni come fluoro, cloro o bromo, modificando la potenza e le caratteristiche chimico-fisiche del composto. Il sevoflurano e il desflurano sono eteri alogenati esclusivamente con fluoro, il che conferisce loro una bassa solubilità nel sangue e una rapida cinetica di induzione e risveglio. A temperatura ambiente, si presentano allo stato liquido e vengono vaporizzati tramite appositi dispositivi nell’apparecchio di anestesia per la somministrazione inalatoria.
Il sevoflurano è ampiamente utilizzato sia per l’induzione che per il mantenimento dell’anestesia, grazie alle sue proprietà broncodilatatorie, risultando particolarmente utile in pazienti con broncopneumopatia cronica ostruttiva (BPCO).
In ambito pediatrico, il sevoflurano è preferito per l’induzione dell’anestesia, poiché evita il trauma dell’incannulamento venoso.
Il desflurano, pur avendo un onset e un offset ancora più rapidi, possiede un odore acre che può irritare le vie aeree, rendendolo meno adatto per l’induzione, ma ideale per il mantenimento dell’anestesia, soprattutto in interventi di breve durata.
Il protossido d’azoto
Il protossido d’azoto (N₂O), noto anche come “gas esilarante“, è un gas non infiammabile ampiamente utilizzato come adiuvante nell’anestesia generale. Sebbene il suo meccanismo d’azione non sia completamente compreso, si ritiene che agisca principalmente come antagonista dei recettori NMDA nel sistema nervoso centrale (SNC), contribuendo così ai suoi effetti anestetici e analgesici.
Il protossido d’azoto è considerato un anestetico a bassa potenza, con una concentrazione alveolare minima (MAC) di circa il 104%. Ciò significa che, per ottenere un’adeguata anestesia nel 50% dei pazienti, sarebbe necessaria una concentrazione inalatoria del 104%, il che è impraticabile poiché comporterebbe una miscela ipossica. Pertanto, viene utilizzato in combinazione con altri anestetici inalatori per potenziarne gli effetti e ridurre le dosi necessarie.
Grazie al suo basso coefficiente di ripartizione sangue/gas, il protossido d’azoto ha un’insorgenza e un recupero rapidi, rendendolo utile per l’induzione e il mantenimento dell’anestesia.
A causa della sua elevata diffusibilità, il protossido d’azoto può accumularsi in cavità corporee chiuse, causando un aumento della pressione al loro interno. Pertanto, è controindicato in condizioni come pneumotorace, enfisema, ostruzione intestinale meccanica e durante procedure come la laparoscopia.
L’uso del protossido d’azoto è stato associato a nausea e vomito post-operatori, probabilmente dovuti all’espansione dello stomaco e dell’orecchio medio. Per ridurre questo rischio, si raccomanda di evitare l’assunzione di cibo nelle due ore precedenti la procedura.
Il protossido d’azoto può potenziare gli effetti di altri farmaci depressivi del SNC, come oppioidi e benzodiazepine, richiedendo un attento monitoraggio durante l’anestesia.
L’uso prolungato o ad alte dosi di protossido d’azoto può interferire con il metabolismo della vitamina B12, portando a potenziali complicanze ematologiche e neurologiche. Pertanto, è importante valutare attentamente i rischi e i benefici nei pazienti con carenze note di vitamina B12 o in quelli sottoposti a procedure prolungate.
Nonostante le sue limitazioni, il protossido d’azoto rimane uno strumento prezioso nell’arsenale anestesiologico, offrendo benefici significativi quando utilizzato in modo appropriato e con le dovute precauzioni.
Effetti sistemici degli anestetici inalatori
- Effetti emodinamici e cardiologici.
Gli anestetici inalatori esercitano effetti emodinamici significativi, principalmente attraverso la depressione della contrattilità miocardica e la riduzione delle resistenze vascolari periferiche. Questi effetti sono dose-dipendenti e possono portare a una diminuzione della pressione arteriosa. In particolare, gli alogenati più recenti, come sevoflurano, desflurano e isoflurano, riducono principalmente le resistenze vascolari sistemiche, con un impatto minore sulla gittata cardiaca. In genere, gli anestetici inalatori hanno uno scarso effetto sulla frequenza cardiaca, ad eccezione del desflurano, che può determinare un aumento della frequenza nelle fasi iniziali della somministrazione, a causa della sua azione bronco-irritante. - Effetti respiratori.
Gli anestetici inalatori influenzano la funzione respiratoria in vari modi. Gli alogenati determinano una riduzione della frequenza respiratoria e della ventilazione alveolare. Solo il protossido d’azoto tende a mantenere una ventilazione spontanea se non somministrato a dosi elevate. È inoltre presente una riduzione dose-dipendente della risposta allo stimolo ipossico ed ipercapnico.
Gli alogenati sono stati utilizzati per la risoluzione dello stato asmatico e determinano una riduzione delle resistenze delle vie aeree, ad eccezione del desflurano, che per le caratteristiche di irritabilità delle vie aeree e il suo odore pungente determina inizialmente un incremento delle resistenze fino a spasmo anche delle alte vie aeree, soprattutto in età pediatrica. - Effetti sul sistema muscolare.
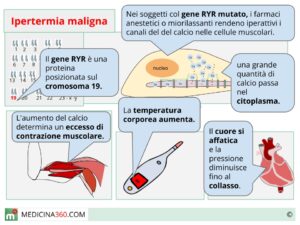
Gli anestetici inalatori potenziano il blocco neuromuscolare degli agenti miorilassanti, riducendo la quantità da somministrare in corso di intervento. Sono tuttavia implicati nell’insorgenza di ipertermia maligna in soggetti predisposti. Il protossido d’azoto non è in grado di potenziare l’attività degli agenti miorilassanti. - Effetti sul sistema nervoso centrale.
Gli anestetici inalatori deprimono l’attività del sistema nervoso centrale, inducendo incoscienza e amnesia. Tuttavia, l’esatto meccanismo d’azione non è completamente compreso e rimane oggetto di studio. - Effetti sul metabolismo.
Alcuni anestetici inalatori, come il protossido d’azoto, possono interferire con il metabolismo della vitamina B12, portando a una sua inattivazione. Questo può avere implicazioni cliniche, soprattutto in pazienti con carenze preesistenti di questa vitamina.
In conclusione, gli anestetici inalatori sono strumenti fondamentali in anestesia generale, con effetti sistemici che devono essere attentamente monitorati per garantire la sicurezza del paziente durante gli interventi chirurgici.
Fonte: