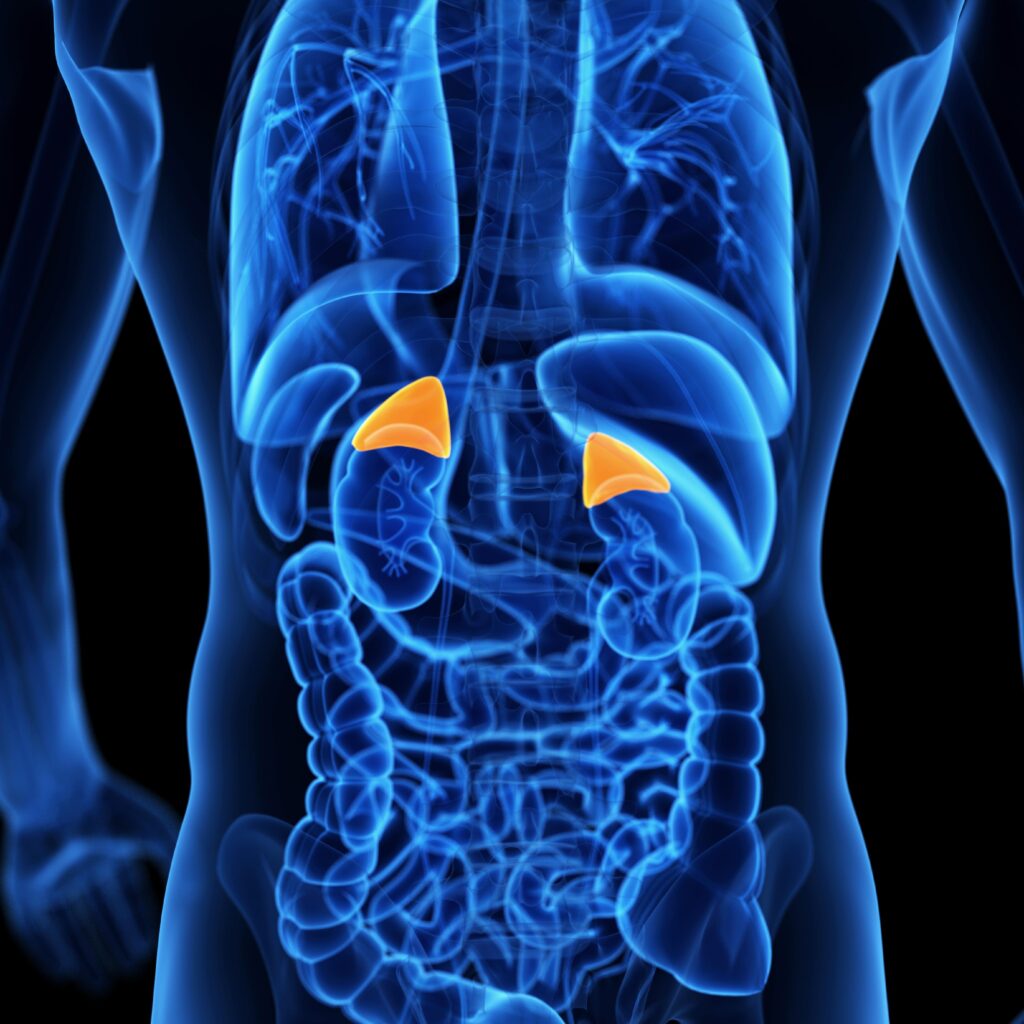
La ghiandola surrenale, piccolo organo endocrino situato sopra ciascun rene, è spesso al centro di indagini diagnostiche complesse. La medicina nucleare, attraverso l’uso di radiofarmaci specifici, offre un contributo fondamentale nella diagnosi, nella stadiazione, nel follow-up e nella valutazione della risposta alla terapia di numerose patologie surrenaliche.
Queste includono i tumori della corteccia (adenoma e iperplasia) e della midollare del surrene (in genere i NET: tumori neuroendocrini), nonché le masse scoperte incidentalmente (incidentalomi).
Non solo: la disciplina riveste un ruolo terapeutico attivo nel trattamento di alcuni tumori, come il neuroblastoma, attraverso la somministrazione di radioisotopi terapeutici.
Applicazioni nella diagnosi dei disturbi della corteccia surrenale
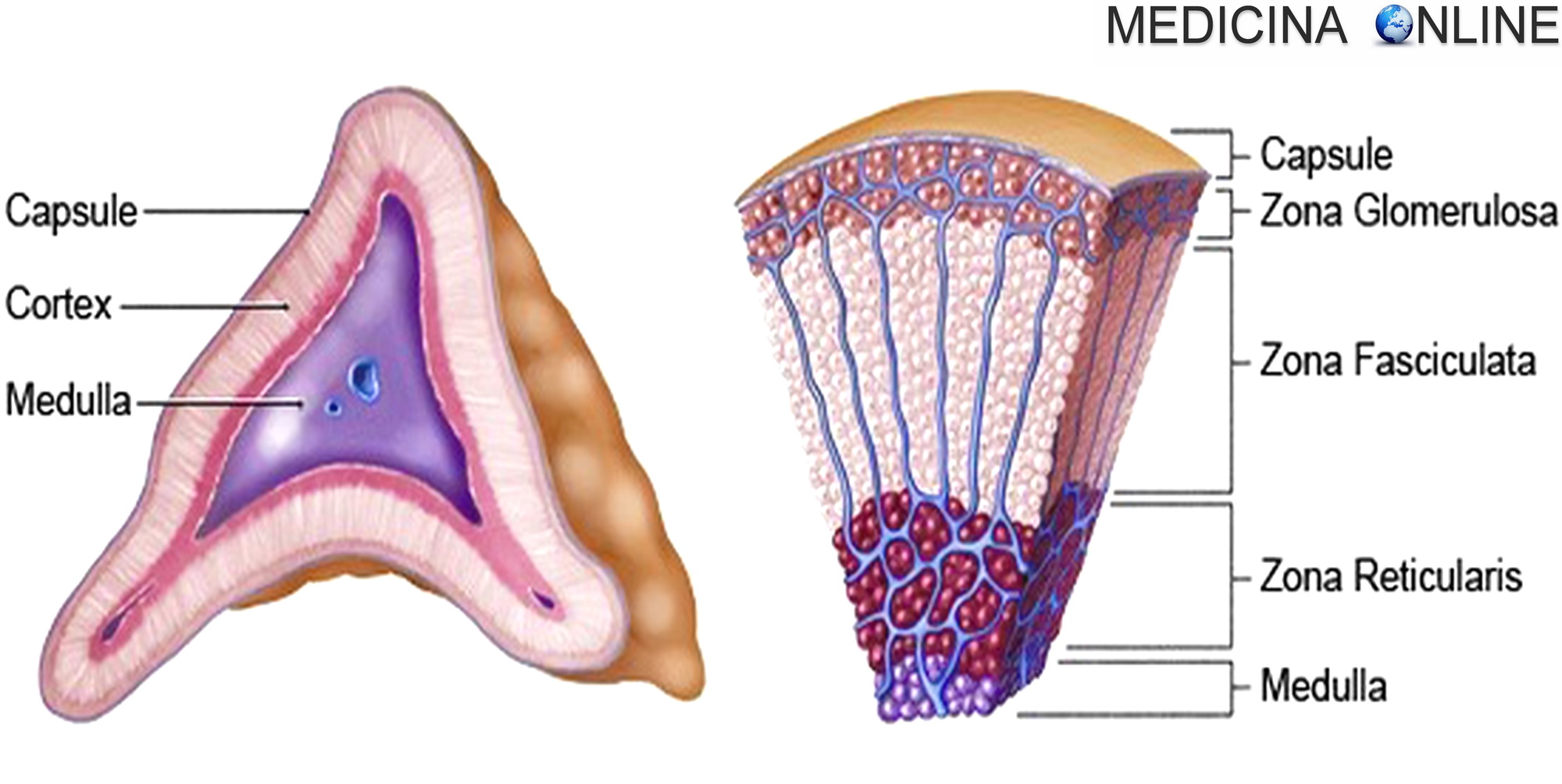
La corteccia surrenale è responsabile della produzione di ormoni vitali come il cortisolo e l’aldosterone. Quando si sospetta un’eccessiva secrezione ormonale (iperfunzione) confermata da esami di laboratorio ma con riscontri radiologici tradizionali (TAC o Risonanza Magnetica) dubbi o negativi, la scintigrafia con un analogo del colesterolo radioattivo, il NP-59 (Iodio-131-6β-iodometil-19-norcolesterolo), diventa cruciale.
Questo radiofarmaco, veicolato nel sangue dalle lipoproteine a bassa densità (LDL), viene captato specificamente dalle cellule della corteccia surrenale che esprimono i recettori per le LDL. L’analisi del pattern di captazione permette di distinguere le diverse cause di iperfunzione:
- un’aumentata captazione unilaterale e precoce è fortemente suggestiva per la presenza di un adenoma, spesso alla base della Sindrome di Conn (iperaldosteronismo primario);
- un aumento dell’attività in entrambe le ghiandole (captazione bilaterale) indica invece un’iperplasia surrenale. Quest’ultima condizione può essere a sua volta causata da un adenoma ipofisario secernente ACTH o, più raramente, da una secrezione ectopica di ACTH da parte di altri tumori.
La valutazione della midollare surrenale e dei Tumori Neuroendocrini
La midollare surrenale, parte del sistema neuroendocrino, è coinvolta nella produzione di catecolamine (adrenalina e noradrenalina). I suoi tumori sono studiati con radiofarmaci altamente specifici.
Studio con MIBG (Meta-Iodo-Benzil-Guanidina)
Il MIBG è una molecola simile alla noradrenalina che si concentra a livello dei granuli di deposito del tessuto adrenergico. I tumori che originano dalla cresta neurale, come il feocromocitoma (localizzato nel surrene) e il neuroblastoma (più comune in età pediatrica), possiedono questi granuli in abbondanza, rendendo il MIBG un marcatore ideale.
Dopo l’iniezione del tracciante (legato allo Iodio-131 o Iodio-123), le immagini vengono acquisite a distanza di 24-48 ore per lo Iodio-131 e 6-24 ore per lo Iodio-123.
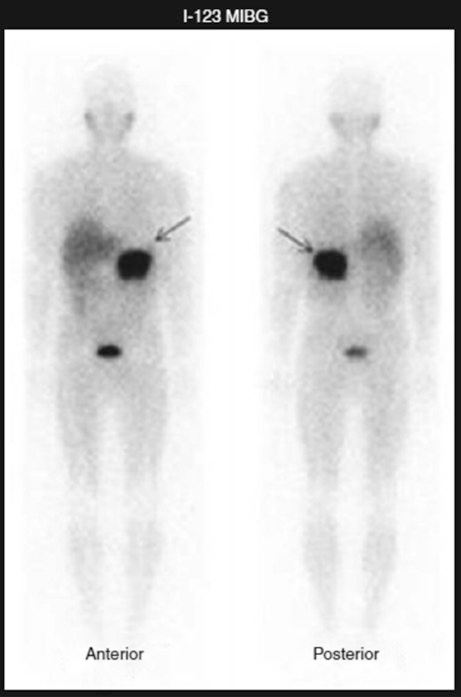
L’esame, oltre a identificare il tumore primario con una sensibilità che supera l’80-90% e una specificità del 90% per il feocromocitoma, è insostituibile per individuare metastasi o recidive di malattia. È importante sottolineare che l’elevata sensibilità del MIBG nel neuroblastoma (circa 91%) non dipende necessariamente da livelli elevati di catecolamine circolanti. Una modesta captazione può avvenire anche in altri tumori neuroendocrini, come il carcinoide e il carcinoma midollare della tiroide.
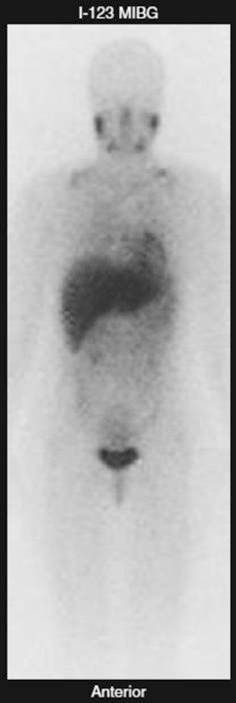
La fisiologica fissazione del radiotracciante avviene al fegato, milza, cuore, ghiandole salivari, intestino, vescica urinaria e grasso bruno.
Caricamento….
Scintigrafia con Octreotide (con Indio-111 o 99m-Tecnezio)
Molti tumori neuroendocrini, incluso il feocromocitoma, esprimono sulla loro superficie recettori per la somatostatina. L’octreotide è un analogo sintetico a lunga emivita di questo ormone, che si lega principalmente ai sottotipi recettoriali 2 e 5.
Questo studio è estremamente utile per visualizzare una vasta gamma di neoplasie, dal paraganglioma al tumore carcinoide. Un’area focale di intensa captazione in sedi non fisiologiche è da considerarsi patologica.
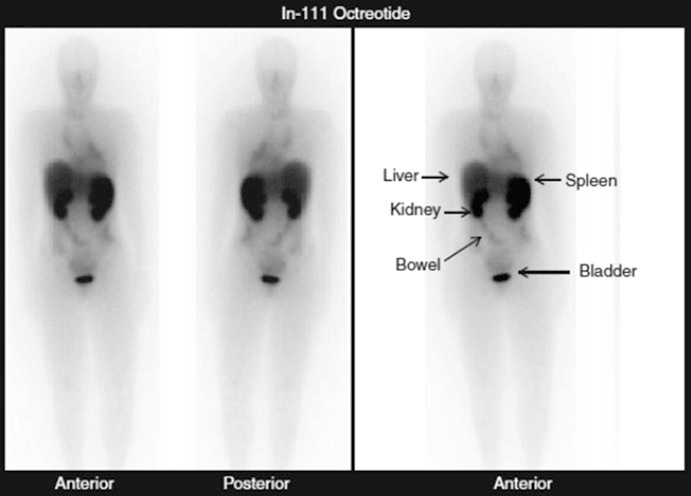
Le normali sedi di fissazione del radiotracciante sono il fegato, la milza, i reni, l’intestino e la vescica.
La tecnica è altamente sensibile per lesioni di dimensioni superiori a 1.5 cm.
Now loading…
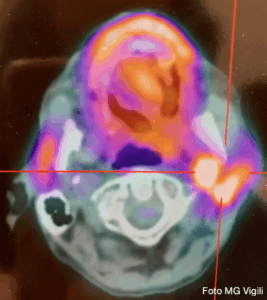
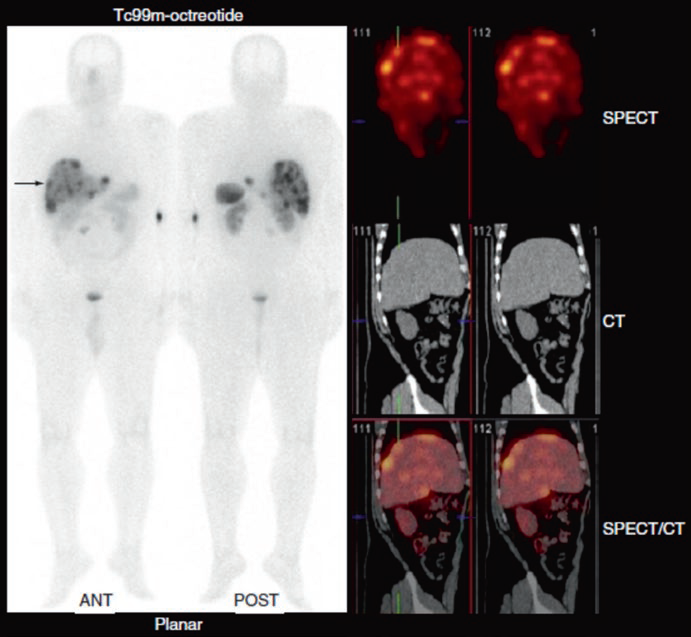
Studio con 99mTc-octreotide eseguito 5 ore dopo l’iniezione, che mostra aree multiple di captazione anomala rappresentanti focolai di tumore carcinoide nel fegato (freccia) nelle immagini planari (a sinistra). Lo studio SPECT/CT (pannello di destra) consente una migliore localizzazione delle anomalie.
Ruolo emergente della PET
La Tomografia a Emissione di Positroni (PET) ha portato una rivoluzione nella caratterizzazione delle patologie surrenaliche, superando i limiti della scintigrafia tradizionale e offrendo una precisione diagnostica senza precedenti. Il suo vero valore non risiede in un singolo tracciante, ma nella possibilità di scegliere la molecola radioattiva più adatta per interrogare la specifica biologia del tumore sospettato, in un approccio “metabolicamente guidato“.
Per le masse surrenaliche di origine incerta, il Fluorodesossiglucosio (18F-FDG) può fornire un primo indizio, in quanto la maggior parte delle metastasi e dei carcinomi surrenalici maligni mostra un metabolismo glucidico molto elevato e quindi un’intensa captazione. Tuttavia, la sua specificità è limitata dal fatto che una significativa percentuale di adenomi benigni, specialmente quelli funzionanti, può presentare un’attività metabolica moderata, generando così falsi positivi e rendendo necessari traccianti più mirati.
La vera forza della PET emerge con i radiofarmaci specifici. Per i tumori della midollare surrenale, come il feocromocitoma, e per i paragangliomi, il tracciante di elezione è 18F-DOPA. Questa molecola sfrutta il pathway metabolico delle catecolamine: viene captata dalle cellule tumorali e convertita in dopamina, mimando esattamente il processo biochimico che caratterizza questi tumori. La PET con 18F-DOPA offre una sensibilità e una specificità che possono superare il 95%, risultando superiore alla tradizionale scintigrafia con MIBG soprattutto nella localizzazione di piccole lesioni e di forme metastatiche.
Un altro pilastro per lo studio dei tumori neuroendocrini è la PET con analoghi della somatostatina marcati con Gallio-68 (come il DOTATATE, il DOTATOC o il DOTANOC). Questa tecnica rappresenta un enorme salto in avanti rispetto alla vecchia scintigrafia con Octreotide. Il Gallio-68 permette un’imaging PET ad altissima risoluzione, in grado di individuare lesioni di pochi millimetri grazie al suo legame estremamente affine con i recettori della somatostatina di sottotipo 2, che sono iperespressi sulla superficie di molti tumori neuroendocrini ben differenziati. Oltre alla straordinaria accuratezza diagnostica, questo esame è fondamentale per selezionare i pazienti che possono beneficiare di una terapia radiorecettoriale peptidica (PRRT) con Lutezio-177, che utilizza lo stesso meccanismo di targeting per veicolare una dose terapeutica di radiazione direttamente alla cellula tumorale.
Infine, per risolvere il dilemma diagnostico degli incidentalomi della corteccia surrenale, è disponibile un tracciante estremamente specifico: il C-11 Metomidato. Questo composto agisce come un inibitore degli enzimi 11β-idrossilasi e aldosterone sintasi, che sono espressi in abbondanza dalle cellule della corticale surrenale ma assenti in tumori di altra origine. Una forte captazione del C-11 Metomidato identifica quindi in modo inequivocabile una massa di origine cortico-surrenalica (che sia un adenoma, un carcinoma o un’iperplasia), distinguendola chiaramente da una metastasi o da un feocromocitoma. Questo lo rende lo strumento ideale per una caratterizzazione biochimica non invasiva del tessuto.
Fonte: A Concise Guide to Nuclear Medicine (Abdelhamid H. Elgazzar e Saud Alenezi)