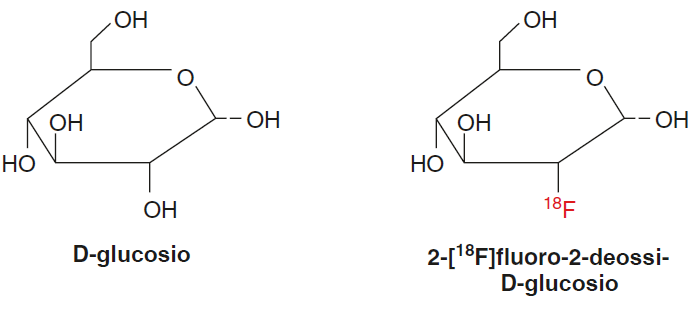
Lo sviluppo clinico dei macchinari PET iniziò seriamente nel 1976 con la dimostrazione che l’analogo del glucosio 2-[18F] fluoro-2-deossi-D-glucosio ([18F]FDG) era sicuro ed efficace per l’imaging dell’utilizzo del glucosio nel cervello umano. [18F]FDG fu concepito come un’estensione in vivo degli ispiratori esperimenti di Sokoloff sulla misurazione del tasso metabolico del glucosio utilizzando 2-deossi-D-[14C] glucosio e l’autoradiografia del tessuto. L’introduzione dell’atomo di 18F in posizione 2 della molecola di glucosio, sostituendo il gruppo idrossile naturalmente presente, è il punto chiave per la sintesi di [18F]FDG.
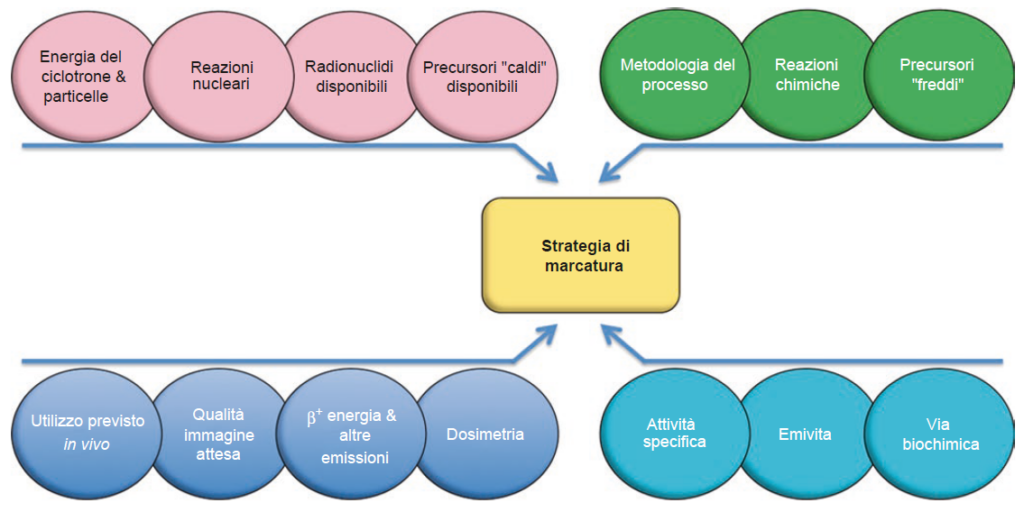
Per raggiungere questo obiettivo è stata progettata una via di sintesi, che utilizzava un substrato predisposto alla marcatura (o “precursore freddo“). La progettazione di una strategia di radiomarcatura va oltre le questioni chimiche e deve considerare l’uso previsto del tracciante.
I requisiti fondamentali nel processo di radiochimica per la sintesi dei radiotraccianti PET sono:
- Scegliere reazioni veloci ed introdurre il radionuclide a breve vita il più tardi possibile nel percorso sintetico (possibilmente come ultimo passo), al fine di limitare la perdita di attività dovuta al decadimento fisico.
- Progettare il substrato (precursore freddo) in modo da favorire la selettività e la specificità della regione (cioè, dirigere la reazione verso il prodotto desiderato e allo stesso tempo evitare/limitare i prodotti collaterali).
- Evitare la presenza di gruppi chimici interferenti/competitivi che possano inibire o influenzare la reazione di radiomarcatura. Di solito vengono utilizzati gruppi protettivi per eliminare le interferenze e dirigere il radionuclide verso una porzione specifica della molecola bersaglio.
Alcuni approcci di marcatura sono diventati “soluzioni classiche”, come l’introduzione di opportuni “gruppi uscenti” nei substrati concepiti per sostituzioni nucleofile del fluoro o l’uso di agenti alchilanti capaci di portare atomi di 11C o 18F.
L’introduzione di elementi, gruppi e frammenti molecolari “esterni” in una molecola biologicamente attiva può influenzare il suo comportamento biologico e la sua accettazione. Il [18F] FDG è stato un chiaro esempio di come la sostituzione di un atomo di fluoro con un gruppo idrossile nella molecola di glucosio abbia trasformato una molecola carburante in un substrato intrappolato nelle cellule. Questo è ancora vero per molti altri analoghi fluorurati di molecole bioattive.
La ricerca di nuovi radiotraccianti PET è in continua crescita e si estende a molti substrati diversi, in particolare substrati proteici. Pertanto, la progettazione molecolare deve considerare l’analisi conformazionale di peptidi, proteine, materiali nanostrutturati e compositi funzionalizzati ad hoc prima di avviare un progetto di marcatura.
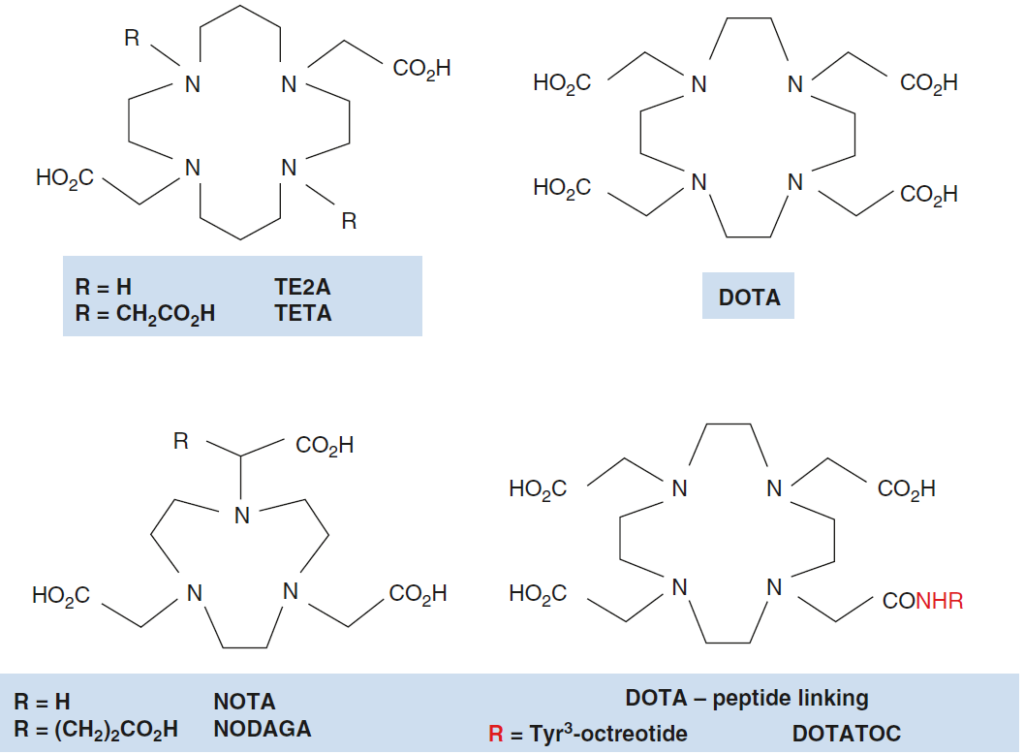
In genere, complessi o chelati di radiometalli emettitori di positroni non possono essere facilmente legati direttamente a una molecola biologicamente attiva. Pertanto, è richiesta l’introduzione di un nucleo chelante adatto nella molecola per etichettare un substrato biologicamente attivo con un radiometallo.
Questi gruppi ponte, comunemente chiamati gruppi prostetici, sono “bifunzionali”, cioè hanno affinità chimica per il substrato da un lato e per il radionuclide dall’altro lato. Sono utilizzati anche per radionuclidi non metallici quando si devono superare ostacoli di chimica tra la chimica del precursore radioattivo e il substrato.
Fonte: Fondamenti di medicina nucleare. Tecniche e applicazioni.

